אי ספיקת כליות היא מצב של התנגדות ל-GH ולא מחסור בהורמון הגדילה (GH).
לפני למעלה מ-50 שנה, סלמון ודואגדיי Salmon 8c Daughaday (1957) [מקור1, מקור2, מקור3] גילו את גורם הגדילה דמוי אינסולין (IGF-I) בעל תכונות איתות דמויות אינסולין ויכולות תווך לפעילויות ביולוגיות שונות בגוף שלנו בהן גדילת רקמות ועצמות, בבקרת מחזור התא – באפופטוזיס בשגשוג, ובהישרדות [מקור1, מקור2], טרנספורמציה, התמיינות, אינטראקציות בין תא לתא ומצע. כך למשל נמצא כי BDNF (גורם הגדילה העצבי) ו-IGF-1 הגדילו שניהם את ההישרדות של נוירוני ההיפוקמפוס (המוח הרגשי) החסרים BDNF, והראו פעולה משלימה לגורמים אלה בתמיכה בהישרדותם [מקור]. IGFs יכולים להתערב גם בהקשר של טיפול במצבים קטבוליים (רצף של תהליכים מטבוליים אשר מפרקים מולקולות גדולות.) הקשורים למחלה. העצמת ה- IGF-I למשל על ידי מתן IGF-I (rhGH – Recombinant) כתרופה – מדובר במתן מולקולות DNA שנוצרו באופן טבעי או תוכננו במעבדה – כתוצאה מצירוף מחדש של מקטעי DNA ממקורות שונים אשר ניתנים לחולים קטבוליים, במצבים חמורים אפשר להפחית בעזרתן את מאזן החנקן השלילי הקשור להגבלה קלורית מתונה [מקור], במצבים של פגיעה בלב נמצא כי ה- IGF-I מקדם התאוששות מאפיזודות איסכמיות היפוקסיות ברקמות לב ועצבים במודלים של בעלי חיים [מקור1, מקור2], מתקן את ההיפרגליקמיה (יתר סוכר) של חולי סוכרת עם תנגודת לאינסולין [מקור], ו
צמיחה של הכליה הנגדית לאחר כריתת כליה חד צדדית.
מערכת GH/IGF1 גם ממלאת תפקיד מפתח בהתפתחות תקינה של הכליות, ויסות המודינמי גלומרולרי, כמו גם טיפול במים צינוריים, נתרן, פוספט וסידן [מקור]. GH ו-IGF-1 ממלאים תפקיד משמעותי בהתפתחות מוקדמת של נפרופתיה סוכרתית, כמו גם במצב של חוסר כליה בצד אחד או בהיפרטרופיה של כליות מפצה לאחר כריתת כליה חד צדדית [מקור1, מקור2, מקור3].
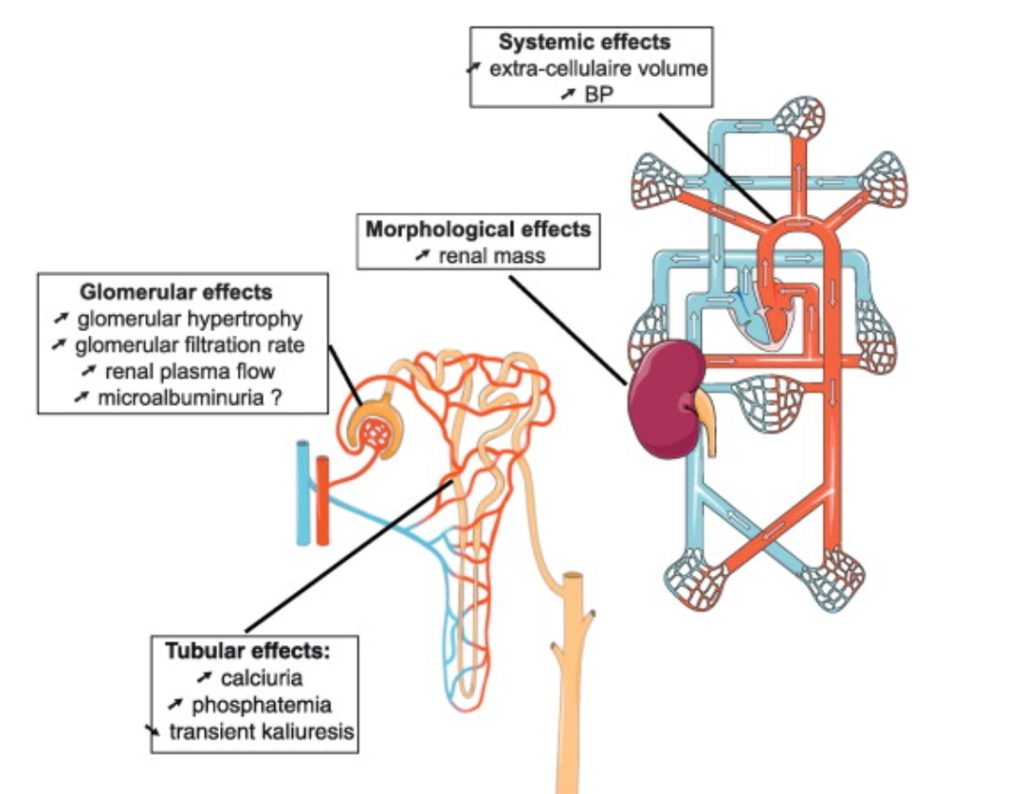
הפרשת יתר סומטוטרופית כלומר הפרשה של בלוטת יותרת המוח הקדמית היא התרופה. נמצאה מאפשרת פעולות שונות של ציר GH/IGF-1 (the somatotropic axis) בכליה: המעודד בהן הוא השפעה נהדרת, טבעית, מדהימה על סינון הכליות האנושית עם עלייה בקצב הסינון הגלומרולרי (GFR).
[מקור]. נושא זה תלוי וקשור במוח הרגשי (ההיפותלמוס) תפקוד לקוי של ההיפותלמוס משנה את התמונה לרעה – על הדרך להזין את המוח נכון פרסמתי כאן – מוזמנים לקרוא.
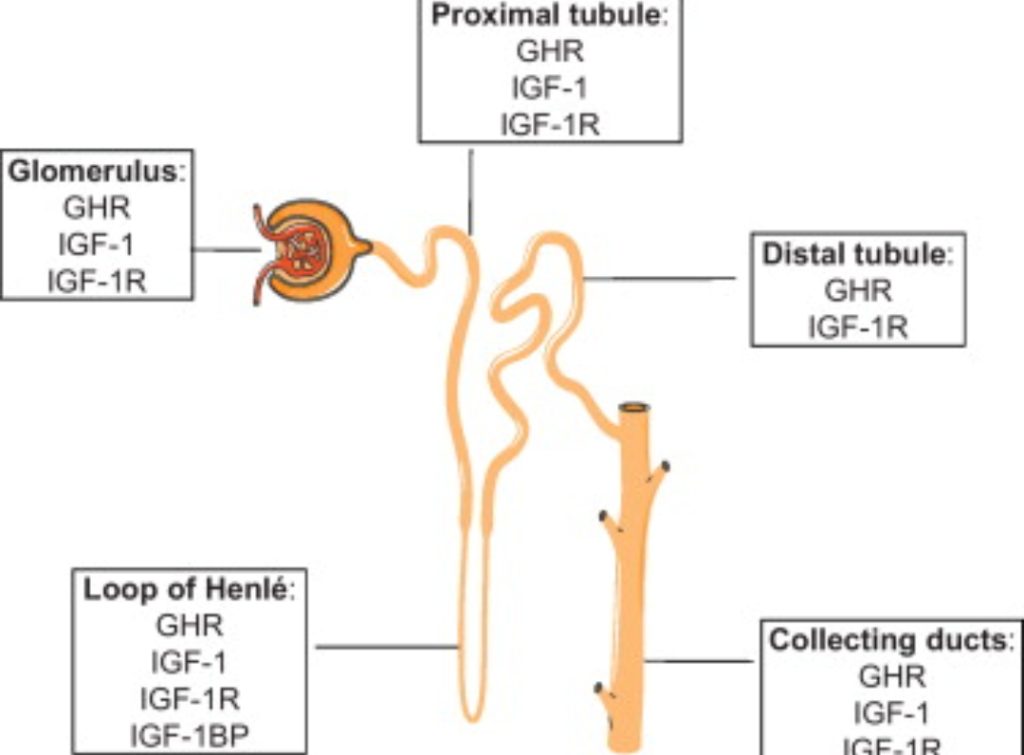
השפעת הפרשת יתר של הורמון גדילה על הכליה. ההשלכות של ההיפראקטיביות של ציר GH/IGF-1 משקפות את מגוון אתרי הפעולה של הורמונים אלו. גנים הורמון גדילה GH (GHR), IGF-1, קולטן IGF-1 (IGF-1R) וחלבוני טרנספורטר IGF-1 (IGF-BP) מתבטאים באופן בולט בכליה הבוגרת בבנאדם, מה שמצביע על תפקיד פוטנציאלי של הציר הסומטוטרופי במגוון תפקודי כליות ומאפשר לחשוב על דרכי פעולה גם להחלמתן. צילום מסך מהמאמר Impact of growth hormone hypersecretion on the adult human kidneyImpact rénal de l’hypersécrétion somatotrope chez l’homme – כאן
הרשימה האינסופית לכאורה של פונקציות המוסדרות על ידי IGFs היא, כמובן, נחמה גדולה לחוקרים המקווים להישאר מועסקים בתחום זה עוד זמן רב. עם זאת, היקף כה רחב של פונקציות הוא בעייתי ביותר כאשר בוחנים את השימושים הטיפוליים הפוטנציאליים עבור IGFs.
גורם הגדילה דמוי אינסולין (IGF-I) הוא חלבון המזרחן שאריות חלבון טירוזין – טירוזין קינאז (קינאז = שפעול של תהליכים בתא על ידי זירחון) טרנסממברני (חוצה דפנות תאים) בתגובה לשינויים במצב הורמון הגדילה (GH) [מקור1, מקור2]. נמצא כממלא תפקיד חשוב בהיפרטרופיה לבבית או בעיצוב מחדש [מקור] מאז, היו הרבה דיווחים על הפעולות של IGF-I ועל הקולטן שלו ( [IGF-IR [מקור]) וכן על חלבוני קושרים (IGFBPs) בוויסות (הסדרה, הַתְאָמָה) תפקודים ביולוגיים במצבים פיזיולוגיים ופתולוגיים כאחד [מקור].
הורמון הגדילה (GH) נקשר לקולטן שלו (GHR), ומייצר השפעות ישירות או עקיפות על ידי גרימת סינתזה של גורם גדילה דמוי אינסולין (IGF-1).
הורמון הגדילה בגוף שלנו מיוצר ומופרש מבלוטת יוֹתֶרֶת הַמּוֹחַ (היפופיזה). [מקור]. הוא מופרש לדם במספר פעימות ביממה, בעיקר בלילה בזמן השינה. הורמון זה מכונה גם סומטוטרופין (Somatotropin), והוא מגרה את גדילת הרקמות בגוף, כולל העצמות [מקור]. ככלל הסומטומדינים (SM) מוגדרים כפפטידים הורמונליים התלויים בהורמון גדילה (GH) ומי שמתווכים פעולת [מקור1, מקור2].
בלוטת יותרת המח! – שאפשר לראות בה את המאסטרו שמנצח על תזמורת, היא אבר כה חשוב עד כי אפשר לומר שאדם אינו מסוגל להתקיים אפילו רגע אחד בלעדיה [מקור]. מערכות רבות בגופנו נשלטות בידי הורמונים. כדי לגדול, לשלוט ברמת הסידן (קלציום) שבדמנו או להפעיל את כל הפונקציות של איברי המין, לכל אלו הגוף חייב להשתמש במערכת משוכללת של שליחים כימיים הקרויים 'הורמונים'. ההורמונים מופרשים ממוקדי יצור שמכונים 'בלוטות'. בגוף האדם פועלות שש מערכות עיקריות של בלוטות ועל מרביתם מנצחת בלוטת יותרת המוח. בלוטה זו היא המנצח היעיל והאחראי על כל פעולות הגוף. ההורמון GH מיוצר בבלוטת יותרת המוח (אצל המאסטרו עצמו) בתאים הסומטו-טרופיים שלה ומגיע ממנה באמצעות זרם הדם אל הכבד [מקור]. כאשר הפרשה עצמה של ההורמון GH על ידי בלוטת יותרת המח [ההיפופיזה (המאסטרו)] נקבעת בעיקר על ידי איזון שמתרחש בין 2 פפטידים: GHRH (מכונה גם somatocrinin) ו -GHIH הידוע גם כ-somatostatin וכן כהורמון מעכב הורמון גדילה [מקור1, מקור2]. סומטוסטטין מעכב את הפרשת אינסולין ואת הפרשת הגלוקגון [מקור1, מקור2]. בנוסף להם מצבי היפרגליקמיה (יתר סוכר הדם) מעכבים את הפרשת GH, והיפוגליקמיה (ירידת רמת הסוכר בדם), תירוקסין, גרלין, קלוטו, וגלוקוקורטיקואידים מעוררים את הפרשת ההורמון GH [מקור]. מכל מקום גם 2 פפטידים אלו מושפעים מגורמים פיזיולוגיים רבים (פעילות גופנית, תזונה, עקה, שינה, יתר/חוסר סוכר) או מעכבים כגון חומצות שומן חופשיות ובהמשך הדרך הדבר משליך על יצירתו של הורמון הגדילה (GH) [מקור]. ההורמון הנולד (GH) ממשיך כאמור אל הכבד. שם הורמון הגדילה נקשר לקולטניו, מה שמעורר פעילות חשובה שבעקבותיה מתרחשת הפרשה של 'פקטור גדילה דמוי אינסולין' (IGF-1). מעתה הוא (IGF-1) שמופרש לדם מככב. פקטור גדילה דמוי אינסולין' (IGF-1) זורם בדם ומגיע ללוחיות הגדילה שנמצאות סמוך לשני הקצוות של כל עצם ארוכה וגורם להתרבות תאי הסחוס שבלוחיות אלו, אזור לוחית הגדילה מורכב מרקמה של תאי סחוס, להם – בניגוד לתאי עצם אחרים – יכולת להתרבות ולהתמתח. בהמשך הדבר מביא להתארכות העצמות ולגדילה. קומה נמוכה נקשרת עם חוסר בהורמון גדילה בילדות ועם קצב גדילה איטי מהמקובל לבני גילם בתקופת הילדות. להורמון גדילה תפקידים נוספים. הוא משפיע על גדילת השריר, ובעזרתו יורדת מסת השומן ועולה מסת השריר. הוא מסייע לכניסת סידן לעצם, פועל לייצור חלבונים וסוכרים ויש לו תפקיד בחילוף החומרים בגוף למשל הוא שמשפיע על אחסון השומן בגוף המרכזי מסיבתו ילד דק גפיים עלול להשמין במרכז הגוף וכן השפעות רבות על עבודת הכליות.
IGF-1 הוא פפטיד קטן (משקל מולקולרי 7647) שמווסת את צמיחת התא, כושר הישרדות ואופני התמיינות על ידי פעולה על הקולטן IGF-I, (IGF-IR) [מקור] הוא מסתובב בסרום במצב קשור לחלבונים (הם קשורים בזיקה גבוהה – 99%) וככזה ה IGF-1 מוגדר פפטיד יוצא דופן מכיוון שהוא קשור ביותר מ-99 אחוז לחלבון [מקור]. רוב ה-IGFs בסרום קשורים ל-IGFBP () ולתת-היחידה הבלתי-לאבילית לחומצה (ALS), חלבון שמייצב את ה-IGF [מקור1, מקור2], כל ששת ה-IGFBP הוכחו כמעכבים את פעולת ה-IGF, אך הוכחו לאחרונה גם השפעות מעוררות של IGFBP-1, –3 ו-5 [מקור]. פעולתו של ה-GH מתבצעת על ידי קשירתו לקולטן GH (GHR). מרגע שהוא נקשר אליו הוא מתחיל לעורר, גנים, ואת הסינתזה – הייצור העצמי של אינסולין גדילה גורם-1 (IGF1) על-ידי הגוף מתחיל [מקור].
IGF-1 מסונתז על ידי מספר סוגי תאים תאי גזע (MSCs – mesenchymal cell types) [מקור1, מקור2]. קיימים שני מנגנונים עיקריים של ייצור IGF-1: IGF-1 המסונתז בכבד ומופרש לדם נמצא ונמצא בשליטה של GH, שהוזכר לעיל, וכן Autocrine/paracrine IGF-1 אשר מסונתז ברקמות היקפיות, כגון העצם או תאי לב [מקור] ותאי כלייה [מקור]. הסינתזה שלו נשלטת על ידי GH ועל ידי גורמים המופרשים באופן מקומי על ידי סוגי התאים שמסביב לאזור הייצור שלו. חלק מה- IGF-1 האוטוקריני/פאראקריני המופרש הוא שנכנס למחזור הדם המערכתי. נושא זה והבנתו מסייעת לפרש שינויים בריכוזי IGF-1 בסרום [מקור]. בנוסף לכך IGF-1 מפעיל את השפעותיו באמצעות הפעלה של הקולטן ל–IGF-1 [מקור]. קולטן זה מופץ באופן נרחב בגוף האדם, מה שמאפשר ל-IGF-1 המועבר בדם לתאם צמיחה מאוזנת בין מספר רקמות ואיברים.
מחקרים אחרונים המשתמשים במודלים של חיות מעבדה (עכבר נוק-אאוט – מחיקת גנים / נוקאאוט פרושו גנים מושתקים [מקור] של רקמה/תא ספציפית וטכניקות תרבית תאים.) הוכיחו בבירור ש
-IGF-I המיוצר באופן מקומי הוא קריטי יותר (בר השפעה מכריעה בהרבה) מה-IGF-I המערכתי שנוצר בכבד.
השפעתו ניכרת למשל, בתמיכה ובפיתוח שלד עוברי ואחרי-הלידה בעיצובה של העצם מחדש [מקור].IGF-1 אוטוקריני/פאראקריני (autocrine/paracrine IGF-1) יכול לעורר צמיחה מקומית, לא מאוזנת ללא תלות ב-GH מערכתית. דוגמאות לסוג זה של ויסות גדילה הן ריפוי פצעים וצמיחה של הכליה הנגדית לאחר כריתת כליה חד צדדית. איתות IGF-I/IGF-IR מקומי מקדם את הצמיחה, ההישרדות וההתמיינות של כונדרוציטים (התאים הבוגרים בסחוס) ותאים יוצרי עצם (אוסטאובלסטים), באופן ישיר ועקיף, על ידי שינוי מסלולי איתות אוטוקריניים/פאראקריניים אחרים בסחוס ובעצם, ועל ידי שיפור האינטראקציות בין תאי השלד הללו באמצעים פיזיים והורמונליים. יתר על כן, איתות IGF-I/IGF-IR מקומי רב השפעה על פעולות העצמות האנבוליות של הורמון הגדילה ועל הורמון הפרתירואיד [מקור]. כל תאי השלד, כולל כונדרוציטים (התאים הבוגרים בסחוס), אוסטאובלסטים, אוסטאוציטים ואוסטאוקלסטים, מבטאים רמות משמעותיות של IGF-I, IGF-II ו-IGF-IR [מקור1, מקור2, מקור3, מקור4]. מולקות אלו מהוות רשתות אוטוקריניות/פאראקריניות מורכבות לוויסות שגשוג, הישרדות והתמיינות של תאים, תוך שליטה בקצב התפתחות הסחוס והעצם והעיצוב מחדש [מקור].
הכליות – מקור הצילום בצילום מסך מהמאמר: "Healthy kidneys, healthy life" כאן
קולטני GH ו-IGF נמצאים גם בכליות ומתבטאים בהן בשפע, כולל בתאים הגלומרולריים שבתוך הכליה ובתאים הצינוריים [מקור]. GH יכול לפעול ישירות על הכליות או באמצעות IGF-1 במחזור הדם או המסונתז על ידי פרקרין [מקור] (פרקרין הוא מולקולה או הורמון המיוצר על ידי רקמה כדי לווסת את הפעילות באותה רקמה. מווסתים פרקריניים נבדלים מווסתים אנדוקריניים, בכך שהם מפרישים חומרים ישירות לזרם הדם, ובכך ניגשים גם לרקמות אחרות [מקור]). ציר או מערכת GH/IGF-1 מווסתת המודינמיקה כליתית וגלומרולרית (נושא שקשור לזרימת הדם בגוף. ציר GH/IGF-1 מסייע לשמור על זרימת דם עקבית המאפשרת מצידה המשך פעולת הסינון ויצירת שתן על-ידי הכליה למרות שינויים מערכתיים בלחץ הדם. גורמים המשפיעים על ההמודינמיקה הכלייתית כוללים את המנגנון האוטו-ויסותי (autoregulatory mechanism – ויסות אוטומטי הוא תהליך בתוך מערכות ביולוגיות רבות, הנובע ממנגנון הסתגלות פנימי שפועל להתאים (או למתן) את תגובת המערכת לגירויים.), כמו כן ציר או מערכת GH/IGF-1 מווסתת את המנגנון הידוע רנין-אנגיוטנסין, את האֵיקוֹסַנוֹאִידים (מולקולות מתקשרות שנוצרות על ידי חימצון של 20 חומצות שומן פחמניות. הן משמשות לשליטה על תהליכים רבים בגוף ובעיקר בגדילה), קינינים (מרחיבי כלי דם בעלי עוצמה; הם מורידים את לחץ הדם וגורמים להתכווצות של שריר חלק. הקינינים ברדיקינין וקלידין נוצרים בדם על-ידי פעולת אנזימים מיוחדים (קליקראין) על גלובולינים של הפלסמה), גם מסייעים לשמור על מערכת העצבים הסימפתטית (SNS), קטכולאמינים ( פועלים כנוירוטרנסמיטורים במערכת העצבים המרכזית, אך גם כהורמונים בדם), הורמון אנטי-דיורטי (מכונה גם וזופרסין הורמון המופרש על-ידי בלוטת יותרת המוח, שמגביר ספיגה חוזרת של מים על-ידי הכליה, וכך מונע איבוד עודפי מים מן הגוף.), אנדותלין שהוא פפטיד מכווץ כלי-דם [מקןר], תחמוצת חנקן, הפפטיד הנטריורטי המוחי Brain natriuretic peptide – BNP פרוזדורי ודופמין.), גלוקונאוגנזה כלייתית [ כליות גם מסנתזות גלוקוז מחלבונים (תהליך המכונה "גלוקונאוגנזה")], צינורית נתרן ומים, פוספט וטיפול בסידן, כמו גם סינתזה כלייתית של 1,25 (OH)2 ויטמין D3 והורמון האנטי-הזדקנות האגדי Klotho [מקור]. על הקלוטו פרסמתי מאמר עומק – כאן הקלוטו המוכר לנו מהציר FGF23-Klotho, בכוחו להשפיע על אורך ועל איכות חיינו, גם על תפקודן של הכליות. הוא פועל גם כקולטן של ההורמון הפוספטורי (phosphaturic hormone – חלבונים המווסתים ספיגה כלייתית של זרחן) גורם גדילת פיברובלסטים – 23 – Fibroblast growth factor באבובית הפרוקסימלית 1α של הכליה (הקרובה לפקעית של הכליה), מפחית את הפעלת ויטמין D, ומגביר את 24-הידרוקסילציה של הכליות (והכבד) של 25(OH)D, מה שמגביר את השבתת ויטמין D [מקור]. רוצה להגיד שחשיבותו של ציר GH/IGF-1 עצומה ורחבה ביותר. על מנת שיפעל כראוי יש לדאוג להזנה נכונה של המוח – על נושא זה פרסמתי – כאן.
למאמרי תובנות חדשות אי-ספיקת כליות תלויה במצבו של ציר FGF23-Klotho
למאמרי מזון למוח – המזון הבריא למוח תומך בגמישות מערכת העצבים שלו וביכולת הלמידה, שומר על הזכרון, ומונע מחלות כגון אלצהיימר – נא להקליק – כאן למאמר.
למאמרי ציר המעיים-מוח – כאן
מקצבים בעולם החי – שעון ביולוגי בתאי הגוף
קשר הגלוטן – אלרגיה לגלוטן והאם הימנעות מגלוטן מוצדקת?
D האם תוסף ויטמין בולם את מחלת הכליות בקרב סוכרתיים?
גלוטמין (Gln) -המגן הגדול על בריאות האדם – כל מה שחשוב לדעת
פיקנוגנול – כל האמת על רפואת עץ האורן והכנת התה ממחטיו
מדד חדש לבריאותך – ביטול האסרוסקלרוזים
בגברים, כ-70% מתפוקת ה-GH היומית מתרחשת במהלך השינה המוקדמת לאורך הבגרות הזכרית. בנשים, השחרור העיקרי של GH תלוי השינה נמוך יותר ומשתנה יותר.
[מקור]
השפעה מאוחרת יותר מופיעה על מבנה הכליה או המורפולוגיה שלה עם עלייה במסת הכליה והיפרטרופיה גלומרולרית,
השפעה האחרונה שנלמדה היא על צינוריות הכליה המובילות להיפרפוספורטמיה (אחת הבעיות הקשות ביותר שהיה עלי להיחלץ מהן כדי להביא להחלמת הכליה, הצטברות של זרחן כתוצאה מתפקוד לקוי של הכליות) והיפרקלציוריה (יתר סידן בדם). [מקור]
מקור האיור בצילום מסך מהמאמר
: Renal effects of growth hormone in health and in kidney disease – כאן
צוות החוקרים E Chin, J Zhou, C Bondy מהמכונים הלאומיים לבריאות, בת'סדה, מרילנד 20892 חקר את הכליה במעבדה על-מנת למחזור את גורם גדילה-I דמוי אינסולין (IGF-I) וגם לזהות את האתר בכליות בו הוא מיוצר כלומר את מקורותיו של ה- IGF-I המקומי כלשון מאמר זה. על מנת לזהות אילו מבנים כלייתיים מייצרים IGF-I ואת חלבון קושר IGF 1 (IGFBP-1) הקשור לתפקוד הכלייתי, וכן את האתרים הפוטנציאליים של פעולת IGF בכליות במחזור או אנדוגני [מקור].
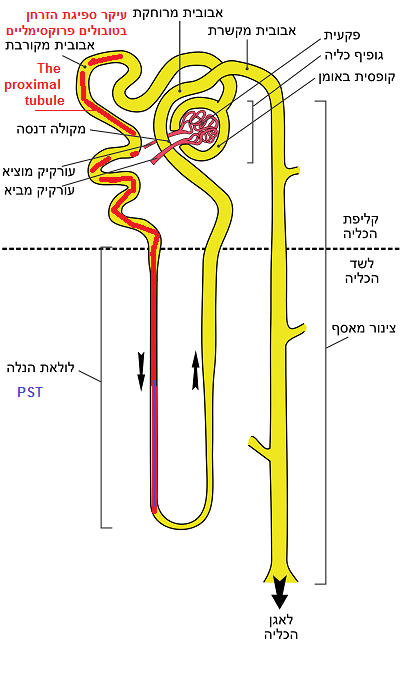
MRNA של IGF-I ו-IGFBP-1 נמצאו בתאי האפיתל של איברים חולים עבים שמורכב מיחידות עצמאיות נפרדות, מדולריות (מודולה היא הליבה הפנימית של הכליה ויש המכנים אותה שלד הכליה) (TALs) של לולאות הנלה בכלייה – היא אחד מחלקי הנפרון (מחלקי הכליות, הנלה אחראית בעיקרה למיהול התסנין. (בנה זו נובעת מבחינה של כליית חולדה רגילה, כלומר לא נוקאאוט). mRNA לקולטן IGF-I נמצא בשפע גם ב-TALs, אך בנוסף, נוכחותו ניכרת גם בכל הנפרון הדיסטלי (מרוחקת) ובצינור האיסוף, וכן בפקעית עצמה בגלומרולוס. רמות נמוכות ביותר נמצאות באבוביות הפרוקסימליות (מקורבת).
GH במחזור משפיע על גודל הכליות מה שבא לידי ביטוי במשקלן.
כשהורמון הגדילה חסר, רואים משקל כליות מופחת
באופן לא פרופורציונלי במעבדה בהשוואה לחיות מעבדה רגילות (עכברים מסוג פרא) [מקור1, מקור2]. רמות גבוהות של GH קשורות להיפרטרופיה כלייתית (גִּדּוּל יֶתֶר) בבני אדם ומכרסמים [מקור1, מקור2]. כיום ברור שציר GH/IGF-1 תורם למחלות כליות מרכזיות כגון נפרופתיה סוכרתית, אי ספיקת כליות, קרצינומה כלייתית (סרטן תאים בהירים) ומחלת כליות פוליציסטית [מקור1, מקור2].
ל-GH השפעות נלוות נוספות בגוף האדם: GH מגביר את אצירת סידן באופן שמחזק ומגביר את תהליך המינרליזציה של העצם; מגביר בתיווך IGF-1 את מסת השריר על ידי הגדלת החלק המתכווץ שלו (מה שידוע כ-sarcomere hypertrophy); מעודד פירוק שומנים-ליפוליזה; מגביר סינתזת חלבונים; מעודד צמיחה וגדילה של כל איברי הגוף הפנימיים פרט למוח; מעודד את מערכת החיסון; תורם לאחזקת ותפקודם של איי בלוטת הלבלב; מפחית קליטת גלוקוזה על ידי הכבד אך מעודד את תהליך gluconeogenesis בכבד; משחק תפקיד ב-homeostasis.
ההפרשה המרבית של GH ו-IGF-1 חלה בשנות הבשלות המינית ואכן באותם שנים תורמים השניים לצבירת ושמירת מסת העצם, במעבר לשנות הבגרות. חסר ב-GH כרוך בירידה במינרליזציה של העצם וצפיפותה (BMD).
GH הוא אחד מסדרת הורמונים התורמים לשמירת רמה נאותה של גלוקוזה בדם. נהוג להתייחס להורמון הגדילה כבעל פעילות anti-insulin כיוון שהוא מדכא את היכולת של אינסולין לעודד קליטת גלוקוזה ברקמות היקפיות, וכן בהיותו מעודד סינתזת גלוקוזה בכבד, ופירוק גליקוגן לגלוקוזה, וכתוצאה מכל אלה מעלה רמת גלוקוזה בדם. באופן מעט פרדוקסאלי מתן הורמון גדילה דווקא מעודד הפרשת אינסולין, מה שמוביל להיפר-אינסולינמיה [מקור].
השפעות של הורמון הגדילה (GH) על הפקעית והצינוריות בכליות
רוב ההשפעות הגלומרולריות והצינוריות של GH מתווכות על ידי IGF-1 וכוללות את הדברים הבאים:
(1) התרחבות של העורקים האפרנטיים והעפרנטיים באמצעות סינתזה מוגברת של תחמוצת החנקן האנדוגנית (NO), וכתוצאה מכך קצב סינון גלומרולרי מוגבר. כלומר ה- GFR עולה. זרימת פלזמה כלייתית;
(2) גירוי של ספיגה חוזרת של פוספט (Pi) בצינוריות הפרוקסימליות באמצעות ויסות מעלה של הטרנספורטרים של נתרן-פוספט (Na-Pi2a/2c;
הערה: פוספטונינים" ( Pi) – Phosphatonins אלו חלבונים המווסתים ספיגה כלייתית של זרחן (בעיקר בממברנה הקודקודית של הצינורית הפרוקסימלית הקרובה לפקעית של הכליה) הם גורמים במחזור הדם שמווסתים את הפרשת הפוספטונינים (Pi) בשתן [מקור] האיור למעלה מתאר את מנגנון הספיגה של הזרחן בצינורית הפרוקסימלית הקרובה לפקעית.
(3) גירוי של ספיגה חוזרת של נתרן (Na+) ומים (H2O) בנפרון הדיסטלי באמצעות ויסות מעלה של תעלת הנתרן האפיתל (ENaC); ו-
(4) גירוי של 1α-hydroxylase ובכך, סינתזת קלציטריול (ויטמין D) באבובית הפרוקסימלית, עם עלייה שלאחר מכן בספיגת הסידן (Ca+) באמצעות ויסות-על של תעלות הסידן האפיתליאליות TRPV6 ו-TRPV5 במעי ובצינורית הכליה הדיסטלית, בהתאמה [מקור].
חלק מהשפעות GH עשויות להיות כמתווך גם על ידי IGF-1, כולל גירוי של (1) הפרשת חומצה נטו באמצעות ייצור מוגבר של אמוניה (NH4+) באבובית הפרוקסימלית ומנגנון תלוי Na+ באבובית הדיסטלית ו-(2) נקשר בסינתזת Klotho הכלייתית, שמתרחשת באבובית הכליה הדיסטלית.
הוכח כי GH משפר ישירות את הגלוקוניאוגנזה הכלייתית בתאים צינוריים פרוקסימליים.
גלומרולוסקלרוזיס – ויתר GH
במצבים של עודף GH יכולה להיגרם בכליה מחלה גלומרולוסקלרוזיס (תסמונת נפרוטית המתאפיינת בהפרשה גדולה של חלבון בשתן, ומובילה בחלק מהמקרים לאי ספיקת כליות מתקדמת – מכונה גם טרשת פקעיתית מוקדית מקטעית) ופציעה של פודוציטים, המאופיינת בהיפרטרופיה של פודוציטים, אפופטוזיס, דה-דיפרנציאציה של פודוקיטים (מעבר אפיתל-מזנכימי, EMT), ו/או קישור צולב של קרום הבסיס, וכתוצאה מכך חדירות פודוציטים מוגברת [מקור]. אלבומין וניתוק פודוציטים מממברנת הבסיס הגלומרולרית. לעומת זאת,
עודף IGF-1 גורם להיפרטרופיה צינורית בלבד.
ההשפעות של כריתת היפופיסקטומיה (Hx) והחלפת GH על ביטוי גנים של IGF-I, IGFBP-1 ו-IGF-I בכליות הוערכו גם כן. MRNA של IGF-I ו-IGFBP-1 ממוקמים שניהם בתאי האפיתל של איברים עולים עבים מדולריים (TALs) של לולאות הנלה בכליית החולדה הרגילה. mRNA לקולטן IGF-I נמצא בשפע גם ב-TALs, אך בנוסף, מופץ בכל הנפרון הדיסטלי וצינור האיסוף, ובגלומרולוס, כאשר הרמות הנמוכות ביותר שלו נמצאו באבוביות הפרוקסימליות.
לטיפול ב-Hx ו-GH היו השפעות מורכבות על דפוסי ביטוי כליות של IGF-I ו-IGFBP-1. באופן כללי, Hx הביא לירידה ברמות ה-IGF-I ולעלייה ברמות ה-mRNA של IGFBP-1, וטיפול ב-GH יצר את ההשפעות ההפוכות, בעוד ש
רמות ה-mRNA של קולטן IGF-I לא הושפעו באופן משמעותי על ידי אף אחד מהטיפולים.
עם זאת, ההשפעה הדרמטית ביותר שנוצרה על ידי הפסקת ציר יותרת המוח-כליה הייתה הדגמה של שינויים הדדיים בביטוי הגנים IGF-I לעומת IGFBP-1 בכליות בודדות ואפילו בנפרונים בודדים, מה נושא זה עולה ומצביע על אינטראקציה מקומית בין IGF-I ו-IGFBP-1 בוויסות רמות ה-mRNA שלהם. השלכות תפקודיות הנובעות מיחסים אנטומיים אלה בדפוסים הכלייתיים של ביטוי גנים לקולטן IGF-I, IGFBP-1 ו-IGF-I הן ש-IGF-I, אם מופרש לתוך לומן הצינורי, אולי נישא או מווסת על ידי IGFBP-1, עשוי לפעול על אתרי קולטנים luminal ו-downstream. התפקיד הפיזיולוגי הספציפי של IGF-I המיוצר ב–TALs פתוח לספקולציות ורב הלא מובן על הידוע. אתרי קולטני IGF-I גלומרולריים, המבוססים על לוקליזציה שלהם במעלה הזרם ומרוחקים ממקורות מקומיים של ייצור IGF-I, צפויים להיות יעדים ל-IGF במחזור. GH רקומביננטי (rhGH – Recombinant) הוא מולקולת DNA שנוצרה באופן טבעי או תוכננה במעבדה – כתוצאה מצירוף מחדש של מקטעי DNA ממקורות שונים שפועל בגוף האדם נמצא בשימוש נרחב בטיפול בקומה נמוכה בילדים, כולל אלו עם מחלת כליות כרונית (CKD).
טיפול בהורמון גדילה רקומביננטי (rhGH) הוכח כבטוח ויעיל בילדים עם CKD.
למרות שהוכח כי rhGH משפר את הצמיחה ומאפשרת לילד להגיע לגובה מבוגר נורמלי, הגובה הבוגר הסופי עדיין נמוך משמעותית מהיעד הגנטי. פיגור בגדילה עלול להימשך לאחר השתלת כליה עקב מספר גורמים, כגון שימוש בסטרואידים, ירידה בתפקוד הכלייתי וציר GH–IGF1 לא תקין. אלה מתחת לגיל 6 שנים הם אלה שהרוויחו הכי הרבה מהשתלה בהדגמת האצה בצמיחה ליניארית. שיטות טיפול חדשות יותר המכוונות לעמידות ל-GH עם IGF-1 אנושי רקומביננטי (rhIGF-1), IGFBP3 אנושי רקומביננטי (rhIGFBP3) ועקירות IGFBP נמצאות בבדיקה ועשויות להתגלות כיעילות יותר בטיפול בכשל גדילה ב- CKD [מקור].
שמו של ה- GH כתוסף פלא רץ לפניו ובהוליווד הוא שיא האופנה [מקור]. במקרים אחדים מדובר בתוסף מאוד יקר. היח"צנים מספרים שהוא מביא לפחות קמטים, להגברת החשק המיני, מעניק יותר אנרגיה (ותוקפנות) [מקור], יחד עם זאת ההשפעת הנלוות של ה-GH בגוף האדם נקשרות בסידן. הורמון הגדילה מגביר את אצירת הסידן באופן שמחזק ומגביר את תהליך המינרליזציה של העצם; הסיבה שצעירים רבים נוהרים אחריו נובעת מכך שהוא מגביר בתיווך IGF-1 את מסת השריר על ידי הגדלת החלק המתכווץ שלו (מה שידוע כ-sarcomere hypertrophy); מעודד פירוק שומנים-ליפוליזה; מגביר סינתזת חלבונים; מעודד צמיחה וגדילה של כל איברי הגוף הפנימיים פרט למוח; בנוסף לכך הורמון הגדילה מעודד את מערכת החיסון; תורם לאחזקת ותפקודם של איי בלוטת הלבלב; מפחית קליטת גלוקוזה על ידי הכבד אך מעודד את תהליך gluconeogenesis בכבד; משחק תפקיד ב-homeostasis. ההפרשה המרבית של GH ו-IGF-1 חלה בשנות הבשלות המינית ואכן באותם שנים תורמים השניים לצבירת ושמירת מסת העצם, במעבר לשנות הבגרות. חסר ב-GH כרוך בירידה במינרליזציה של העצם וצפיפותה (BMD).GH הוא אחד מסדרת הורמונים התורמים לשמירת רמה נאותה של גלוקוזה בדם. נהוג להתייחס להורמון הגדילה כבעל פעילות anti-insulin כיוון שהוא מדכא את היכולת של אינסולין לעודד קליטת גלוקוזה ברקמות היקפיות, וכן בהיותו מעודד סינתזת גלוקוזה בכבד, ופירוק גליקוגן לגלוקוזה, וכתוצאה מכל אלה מעלה רמת גלוקוזה בדם. באופן מעט פרדוקסאלי מתן הורמון גדילה דווקא מעודד הפרשת אינסולין, מה שמוביל להיפר-אינסולינמיה [מקור].
נשארו לך שאלות
אשמח להשיב על כל שאלה
לטופס פנייה ישירה אל ירון מרגולין – נא להקליק – כאן
בבקשה לא להתקשר משום שזה פשוט לא מאפשר לי לעבוד – אנא השתמשו באמצעים שלפניכם –
למען הסר ספק, חובת התייעצות עם רופא (המכיר לפרטים את מצבו הבריאותי הכללי של כל מטופל או שלך) לפני שימוש בכל תכשיר, מאכל, תמצית או ביצוע כל תרגיל. ירון מרגולין הוא רקדן ומבית המחול שלו בירושלים פרצה התורה כאשר נחשפה שיטת המחול שלו כבעלת יכולת מדהימה, באמצע שנות ה – 80 לרפא סרטן. המידע באתר של ירון מרגולין או באתר "לחיצות ההחלמה" (בפיסבוק או MARGOLINMETHOD.COM ), במאמר הנ"ל ובמאמרים של ירון מרגולין הם חומר למחשבה – פילוסופיה לא המלצה ולא הנחייה לציבור להשתמש או לחדול מלהשתמש בתרופות – אין במידע באתר זה או בכל אחד מהמאמרים תחליף להיוועצות עם מומחה מוכר המכיר לפרטים את מצבו הבריאותי הכללי שלך ושל משפחתך. מומלץ תמיד להתייעץ עם רופא מוסמך או רוקח בכל הנוגע בכאב, הרגשה רעה או למטרות ואופן השימוש, במזונות, משחות, תמציות ואפילו בתרגילים, או בתכשירים אחרים שנזכרים כאן.
מאמרים אחרונים
- השפעות של הורמון הגדילה (GH) על תפקוד הכליות בבריאות ובמחלות כליות
- anti-GAD – הנוגדנים העצמיים כנגד האנזים GAD על פני תאי ביתא בלבלב הם נציגי השטן עצמו בגוף האדם ומקור למספר רב של מחלות קשות בהן סוכרת מסוג (T1D) 1, ירידה בתפקוד בלוטת התריס, הפחתה בגאבא המיוצרת בתאי המוח מגלוטמט, התקפי חרדה ואפילפסיה
- בלוטת התריס -מחסור ביוד, חוסר סלניום או עודף פלואור במים גם דמימה בשרירים שנצמדים לעצם הלשון עלולים להוביל לתת פעילות של בלוטת התריס (תירואיד)
- מסלול איתות חדש במוח שמווסת אכילה מופרזת
- דיכאון וחרדה בקרב חולי כליות
- גמילה מאלכוהול – תהליך קשה, תסמינים איומים
- חילוף חומרים אנרגטי, איזון רקמת השומן ובקרת תיאבון
- מחסור ביוד, חוסר סלניום או עודף פלואור במים גם דמימה בשרירים שנצמדים לעצם הלשון עלולים להוביל לתת פעילות של בלוטת התריס (תירואיד)
- מסלול איתות חדש במוח שמווסת אכילה מופרזת
- דיכאון וחרדה בקרב חולי כליות
- עורקים גמישים – הסוד והדרך לזכייה בבריאות מחדש
- יש פתרון כולל לבעיות הקשורות לדימוי עצמי, חוסר בטחון וערך עצמי נמוך – דופמין
- שיחות ההחלמה ושיחות בין ידידים – על ההבדלים ביניהן
- משחה צהובה – לכאבי שרירים – משחת הפלא להפחתת כאבים
- לסדרת מאמרי – מבוא לתורת הגוף-נפש המודרנית – חלק א
- הפסיכולוגיה הטיפולית וההוליסטית – תולדות הפסיכותרפיה
- הגיל השלישי, תאוותיה של הזיקנה – ואיך להתבגר יפה, טוב ובריא
- בני-על – האם יש גבול ביולוגי למספר השנים שאדם יכול לחיות?
- כל מה שאתה צריך לדעת על מיקרו-תזונה – ויטמינים ומינרלים
- הפרעה אנדוקרינית
- חרדה
- מגילת רות האלמנה שיצאה ממרחב הנוחות
- איך מורידים לחץ וחרדות באופן טבעי? התמודדות עם סטרס ולחץ נפשי
- טיפול נפשי ללא תרופות – חרדות, פחדים וייאוש – תסמינים שיש להם פתרון טבעי, מדויק ומהיר
- מסלול ההתפתחות הנורמטיבי בחיי אדם ודמימותיו בטבלה – סדרת מאמרים.
- למה אני לא מצליח להתמיד – והסוכר
- על ההזנחה –
- גמישות היא מצב נפשי – אתגר בזרימה ושינוי – אני מבקש להתגמש
- חזרה לבסיס – עקרונות צירופי המזון
- ניתוק רגשי – על הקורוציונה
- די לכאב
- ראיית המעמקים – כניסה לטרקלין או על החיים האמתיים.
- התודעה השלילית
- ביקורת מבזה
- איך לצאת ממצבי תקיעות בחיים – שיטת שלוש השאלות בגובה העיניים
- נמאס לי מהחיים מה עושים
- על היכולת להשתקם, לקום מאבק הדרך ומכאב הפרידה
- ירקות ירוקי עלים לרוב טובים לבריאותנו, לפעמים הם לא – רוצה לדעת מתי כדאי לצרוך עלים ירוקים?
- תרופות ללחץ דם גבוהה נמצאו כקשורות לסיכון מוגבר לסכיזופרניה
- מדד חדש לבריאותך – ביטול האסרוסקלרוזים
- לראשונה, מדענים הצליחו לתרגם לטקסט את הפעילות המוחית של אדם עם שיתוק שאינו מסוגל לדבר.
- רוצה להחלים בצורה פשוטה ביותר, ללא תרופות ממחסור בטסטוסטרון או מירידה במדד ה SHBG ?
- אוראה – למה האוראה מוגברת ומופחת בדם Urea
- טיפולים מבוססי רירית לזיהומים נגיפיים וחיידקיים
- מחסור בברזל
- קרום התא – הממברנה והדלקת הכרונית
- מחלת שינוי מינימלי Minimal Changes Disease מינימל צ'יינג'
- מה היא בדיקת D-dimer
- חלב לקוליטיס כיבית: כל מה שחשוב לדעת
- המפריעון Vaxinia – CF33 בפעם הראשונה הוזרק בניסוי קליני וירוס קוטל תאי סרטן.
- סטרס יכול לעתים גם לרפא – מחקר חדש על תאי המוח
- רככת היפופוספטמית (זרחן נמוך מהנורמה) – מחלת כליות כרונית – או הפרעת עצם מינרלית
- אי ספיקת כליות – הגורמים השכיחים ביותר ל-CKD הם סוכרת שנשלטת על ידי תרופות = שליטה גרועה בסוכרת ויתר לחץ דם שמטופל לכאורה על-ידי תרופות
- מחלת כליות פוליציסטית אוטוזומלית דומיננטית (ADPKD)
- גמילה מאלכוהול – תהליך קשה, תסמינים איומים
- הגל החדש של בדיקות דם בהחלט רוצה לייעל את הביצועים הספורטיביים שלך, לשפר את הרווחה הכללית ולהרחיב או להאריך את תוחלת החיים גם לסייע להחלמתך ללא תרופות ממחלות כרוניות
- מדללי דם טבעיים – חומרים אנטי-תרומבוטיים: נאטוקינאז, ויטמין E, פלפל קאיין, כורכום, קינמון, וספורט מאפשרים טיפול בנוזלי הדם ללא תרופות.
- סלניום Se התגלה כאנטי- אייג'ינג ומגן מפני מחלות כרוניות
- מהו אימון שלפוחית השתן?
- פסוריאזיס, האם הימנעות מגלוטן מסייעת לחולי הפסוריאזיס
- חלב לקוליטיס כיבית: כל מה שחשוב לדעת
- המפריעון Vaxinia – CF33 בפעם הראשונה הוזרק בניסוי קליני וירוס קוטל תאי סרטן.
- סטרס יכול לעתים גם לרפא – מחקר חדש על תאי המוח
- רככת היפופוספטמית (זרחן נמוך מהנורמה) – מחלת כליות כרונית – או הפרעת עצם מינרלית
- אי ספיקת כליות – הגורמים השכיחים ביותר ל-CKD הם סוכרת שנשלטת על ידי תרופות = שליטה גרועה בסוכרת ויתר לחץ דם שמטופל לכאורה על-ידי תרופות
- מחלת כליות פוליציסטית אוטוזומלית דומיננטית (ADPKD)
- גמילה מאלכוהול – תהליך קשה, תסמינים איומים
- הגל החדש של בדיקות דם בהחלט רוצה לייעל את הביצועים הספורטיביים שלך, לשפר את הרווחה הכללית ולהרחיב או להאריך את תוחלת החיים גם לסייע להחלמתך ללא תרופות ממחלות כרוניות
- מדללי דם טבעיים – חומרים אנטי-תרומבוטיים: נאטוקינאז, ויטמין E, פלפל קאיין, כורכום, קינמון, וספורט מאפשרים טיפול בנוזלי הדם ללא תרופות.
- על הנקמה – פנטזיות נקמה לאחר חווית אירועים טראומטיים
- מסלול ההתפתחות הנורמטיבי בחיי אדם ודמימותיו בטבלה. עמוד 18
- מסלול ההתפתחות הנורמטיבי בחיי אדם ודמימותיו בטבלה. עמוד 17
- המפריעון Vaxinia – CF33 בפעם הראשונה הוזרק בניסוי קליני וירוס קוטל תאי סרטן.
- סטרס יכול לעתים גם לרפא – מחקר חדש על תאי המוח
- אי ספיקת כליות – הגורמים השכיחים ביותר ל-CKD הם סוכרת שנשלטת על ידי תרופות = שליטה גרועה בסוכרת ויתר לחץ דם שמטופל לכאורה על-ידי תרופות
- גאוט הוא לא רק יתר פורין – החיים עם גאוט תלוי גיל ומין – האם אפשר לנצח גאוט בלי לבלוע הורמוני מין?
- גלוטתיון כל האמת
- תרופות הרגעה שמשאירות אותך רעב וחרד – ציפּרָלֵקס, פּרוֹזַק, פלואוקסטין
- גלוטמין (Gln) -המגן הגדול על בריאות האדם – כל מה שחשוב לדעת
- פיקנוגנול – כל האמת על רפואת עץ האורן והכנת התה ממחטיו
- תחמוצת החנקן (NO) כיווץ תאי האנדותל, מחלות כרוניות קשות – ודרכי ריפוי חדשות
- מחשבון מדידה והערכת קצב הסינון הגלומרולרי (GFR) אשר מבוסס על קריאטינין, נתוני גוף, גיל, גזע ומין.
- אומגה 3 צמחית (שמן חרדל, שמן מרווה מרושתת) עולה על צורות אחרות של אומגה 3 ויש והן לבדן תורמות לבריאות בעוד האחרות עלולות להזיק יותר משלהועיל לך
- התכנית לשיקום הכליות פרק ז' – עקרונות הטיפול
- התכנית לשיקום הכליות פרק ו' – התבוננו אל מדד האוראה
- התכנית לשיקום הכליות פרק ה' תנגודת לאינסולין
- התכנית לשיקום הכליות פרק ד'
- התכנית לשיקום הכליות פרק ג
- התכנית לשיקום הכליות פרק ב
- התכנית לשיקום הכליות – פרק א'
- אכל נקי
- אי ספיקת כליות – טיפול ללא תרופות
- על ההשפעה האיומה של חלבון מן החי על הכליות
- אילוף הכליות הסוררות
- גודש נוזלים בריאות – בקרב חולי כליה
- עשרת המזונות הבריאים ביותר לחולי כלייה – קמח קליפת רימונים (PPF) .9
- הגיל השלישי, תאוותיה של הזיקנה – ואיך להתבגר יפה, טוב ובריא
- רוצה להחלים בצורה פשוטה ביותר, ללא תרופות ממחסור בטסטוסטרון או מירידה במדד ה SHBG ?
- רעלים אורמיים מקדמים דיאליזה – הוכח לאחרונה שרעלנים אורמיים קשורים למיקרוביוטה של המעי הגס – איך להחלים ללא תרופות ולהימנע מדיאליזה.
- רככת היפופוספטמית (זרחן נמוך מהנורמה) – מחלת כליות כרונית – או הפרעת עצם מינרלית.
- גודש נוזלים בריאות – בקרב חולי כליה
- דלקת כליות אינטרסטיציאלית – השתמשו במי שעורה
- יתר לחץ דם – שינוי פרדיגמה וגישות חדשות – לחץ דם גבוה וטיפול טבעי ללא תרופות לאחר שטיפול תרופתי נערץ כשל
- הומוציסטאין, ויטמינים ומניעת מחלות כלי דם
- פרפור פרוזדורים (A-fib) יכול להפסיק מעצמו.
- טיפול בכאב עם אופיואידים גורר אותך לצרות צרורות למשל עצירות איומה. מה לעשות?
- גאוט הוא לא רק יתר פורין – החיים עם גאוט תלוי גיל ומין – האם אפשר לנצח גאוט בלי לבלוע הורמוני מין?
- חומצה אלפא לינולנית משפרת את תוחלת החיים – צריכה גבוהה של חומצות שומן מצמחים נחשפה כגורם שמאריך את החיים.
- תובנות חדשות אי-ספיקת כליות תלויה במצבו של ציר FGF23-Klotho
- Tsamba שתי כוסות גרגרי שעורה דגנים מלאים, רצוי אורגניים – מתכון צ'מפה למבקשים להחלים מאי ספיקת כליות
- פאראצטמול (PARACETAMOL) גם פרצטמול או אצטאמינופן (Acetaminophen) – הידוע גם בשם אקמול, רוקסט ודקסמול עלול לפגוע בכליות ובכבד ואסור לשימוש לחולי כליה
- מקצבים בעולם החי – שעון ביולוגי בתאי הגוף
- מעגל המוזר – התפתחות ה"אני" בשנה התשיעית לחייו

כתיבת תגובה