
הצטברות חלבונים רעילים – גושי חלבונים שמצטברים מאפיינים מחלות ניווניות של המוח כמו אלצהיימר נחשבו עד עתה לבלתי הפיכים. החידוש בכך שמסתבר שהגושים נעלמים
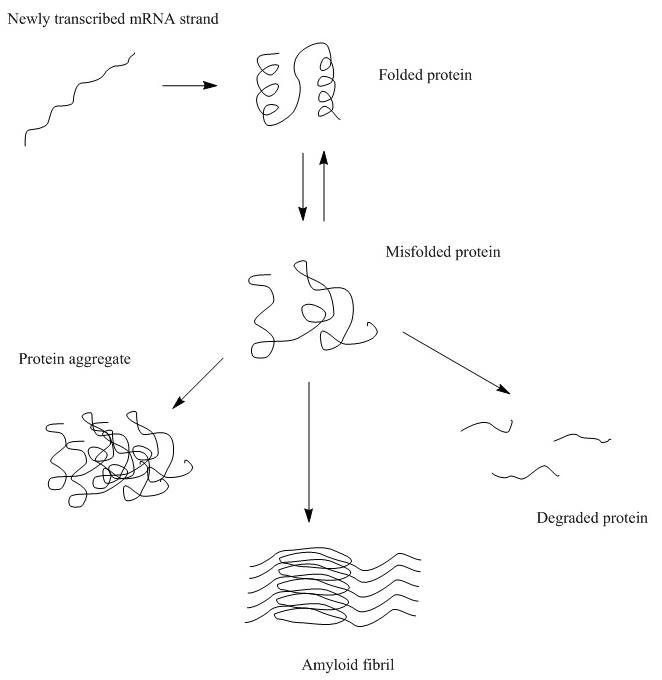
עודף של חלבונים לא תקינים יכול לגרום לפעילות אנזימטית לא רצויה ולצברי חלבונים פגומים בחלל התא ובממברנה. צבירים אלה נקראים אגרגטים (aggregates – איור שני מכאן למטה – בירוק) [מקור]. במוחם של חולים עם מחלות נוירודגנרטיביות, חלבונים אלה, האגרגטים מצטברים [מקור]. הם יכולים להזיק לתאי העצב שהפעילות הממברנלית שלהם דורשת סדר מבני בממברנה וששלוחותיהם יכולות להיסתם בגללם. אגרגטים מעורבים במגוון רחב של מחלות הידועות בשם עמילואידוזות, כולל ALS, אלצהיימר, פרקינסון ומחלת פריון [מקור1, מקור2, מקור3]. המחלה אלצהיימר נקראת על שמו של אלואיס אלצהיימר, פסיכיאטר בווארי מומחה בנוירופתולוגיה, שפרסם בשנת -1906 מקרה בו מטופל, אוגוסט ד', אישה בת 51, שעורר שינוי פרדיגמה גדול באופן שבו אנו חושבים על הפרעות נפשיות עד היום ("Uber eine eigenartige Erkankung der Hirnrinde" אלצהיימר, 1907). אלצהיימר טען כבר אז שהדמנציה שלה ("דמנציה פרסנילית") קשורה קשר הדוק לנגעים נוירופתולוגיים חמורים שצפה בהם במוחה בניתוח שלאחר המוות. אלצהיימר כינה אותם: "גופים צבאיים" (“miliary bodies”) ותאי עצב שחלקם הפנימי נחנק על ידי "צרורות צפופות של סיבים". הדו"ח שלו הצביע על פלאקים ייחודיים וסבך נוירו-פיברילרי בהיסטולוגיה של המוח. המחקר התקדם ומתוך נתיחות מוח של רוב מקרי הסניליות משנות ה- 60 ואילך ברמה המיקרוסקופית ניכרו משקעים חוץ-תאיים של β-עמילואיד (הוא מונח בביוכימיה המתאר משקע בלתי מסיס של חלבון [מקור]. באותה תקופה אלו כונו ה"מוקדים המיליאריים" של אלצהיימר) בנוסף לכך החלו מזהים משקעים תוך-תאיים של סבכים נוירו-פיברילריים ("צרורות צפופים של סיבים" כפי שאלצהיימר כינה אותם [מקור1, מקור2]. סיבים עמילואידים הרסניים שאלצהיימר גילה הם החלבונים שקופלו בצורה לא נכונה והצטברו. צבירים אלה נקראים כיום האגרגטים.
מדענים ממכון מקס פלנק לביוכימיה במרטינסרייד, בראשות מארק היפ ואולריך הארטל, הראו לאחרונה שמיקומם של אגרגטי חלבון אלה משפיעים גם על יכולת ההישרדות של תאים. בעוד האגרגטים שנמצאים בתוך הגרעין בעלי השפעה אפסית על תפקוד הסלולר, הפקודות של החלבונים הלא תקינים האלה בתוך הציטופלסמה (הנוזל של התא) מפריעים לנתיבי תחבורה חשובים בין הגרעין לבין הציטופלזמה עצמה. נושא זה הוא אחד היסודות למחלות נוירודגנרטיביות, כמו אלצהיימר, פרקינסון, או הנטינגטון [מקור].
מחקר פורץ דרך נוסף נערך במעבדה של פרופ' מרטין קופייק מבית הספר לביולוגיה מולקולרית וביוטכנולוגיה באוניברסיטת תל אביב. תוצאות המחקר התפרסמו בכתב העת Molecular Cell (דצמבר 2017) [מקור].
"גושי חלבונים, או אגרגטים, נוצרים בתאים", מסביר ד"ר קובי סימפסון-לביא שערך את המחקר במעבדתו של פרופ' קופייק. "הגושים האלה נוצרים מסיבות רבות, וזה נחשב (עד לאחרונה) למצב בלתי הפיך. התופעה אופיינית למספר מחלות קשות, ובמיוחד למחלות המתאפיינות באבדן תפקוד מוחי".
ככלל, רוב התהליכים בתוך התאים שלנו מבוצעים על ידי חלבונים. בדרך כלל, אלו הן מולקולות מסיסות המסוגלות לעבור ממקום למקום בתא. גושי חלבונים לא תקינים משבשים את היכולת הזאת וגוררים את הגוף למספר מחלות, שהוזכרו: סוכרת, אלצהיימר, פרקינסון, וספגת המוח ("הפרה המשוגעת") בהמשך גם לאי ספיקת כליות. התאים מנסים לפרק את הגושים האלו, או לערום אותם במקומות מסוימים בתא כדי למזער את ההפרעה.
סוכר כזרז מחלה – במחקר (2017) של, ד"ר סימפסון-לביא נבחנה התגובה של תאי שמרים לנוכחות סוכרים, ונמצא שהוספת גלוקוז (סוכר) למצע הגידול גורם להיערמות של חלבון בשם Std1.
כאשר רמות הסוכר בתא ירדו, הגושים נעלמו והחלבון Std1 חזר למיקומו הטבעי בגרעין, שם נמצא הגנום של התא, אומר פרופ' קופייק [מקור]. מכיוון של- Std1 תפקיד מרכזי בתגובה, לנוכחות סוכרים שונים במצע הגידול משמעות רבה, נראה שהאגרגציה (הצטברות החלקיקים על-מנת ליצר יציבות בתא) ההפיכה שנחשפה, היא מנגנון בקרה, שמלמד על האפשרות שעומדת לתאים להגיב במהירות לרמות משתנות של סוכר בסביבת הגידול. מה שמעלה את האפשרות שלא כל הצטברות של חלבון גורמת למחלה, וש
אפשר אולי להפוך אגרגציה לא הפיכה להפיכה.
מדענים בראשות צוות במכון המחקר לדמנציה בבריטניה, באוניברסיטת קיימברידג', הצטרפו למהלך וגם הם הראו שתהליך זה שהתגלה לאחרונה, עשוי לסייע במניעת הצטברות של סבכי חלבון (הנראים בדרך כלל בדמנציה), על ידי היפוך הצטברות של אגרגטים, לא על ידי סילוקם לחלוטין, או בעזרת הפחתת גלוקוז, אלא על ידי "קיפולם מחדש" [מקור]. נושא זה מאפשר "למנוע רעילות של אגרגטים", אמר ד"ר אבזוב ל-MNT [מקור]. ההדגות של הכותב (ירון מרגולין)

סלניום – Se [מקור] מופיע בשתי צורות: הראשונה אורגנית (סלנו-מתיונין וסלנו-ציסטאין) ושתיים אנאורגנית (selenate ו-selenite) [מקור]. בקרקע (באדמה) מופיע סלניום בצורתו השנייה האנאורגניות, וכאשר צמחים קולטים אותו, הם הופכים אותן לצורותיו האורגניות, סלנו-מתיונין (selenomethionine) וסלנו-ציסטיאן (selenocysteine) וכן לנגזרי המתיל שלהן. בגוף האדם הסלניום מהווה מרכיב של חומצות האמינו שנובעות מהמתיניון. רוב המתיונין (היא אחת מ-20 חומצות האמינו הנפוצות בטבע. חומצה חיונית לגוף האדם.) מופיע בצורת סלנו-מתיונין (selenomethionine), ובצורתו זו גם הוא יכול להשתרבב אל תוך חלבוני הגוף כשהוא ממלא תפקיד מפתח בשליטה והסרת הצטברות או אגירה של חלבונים רעילים – חלבונים מקופלים שגויים [מקור, מקור2, מקור3, מקור4].
החלבונים הם מולקולות שמבצעות את רוב העבודה בתאי גופנו. כאשר חלבון מסונתז בתא על ידי הריבוזום, הוא נמצא במבנהו הראשוני, כלומר כשרשרת ארוכה של חומצות אמינו ללא מבנה מוגדר. במצב זה החלבון אינו פעיל ולא יכול לבצע את עבודתו. כדי למלא את ייעודו על החלבון להתקפל (Protein folding) [מקור]. תהליך הקיפול יוצור מבנה תלת-ממדי. מבנה כזה מבנה נטיבי (Native state), והוא בעל מבנה שלישוני או רביעוני, מקופל במבנה תלת ממדי. חלבונים בעלי קיפול שגוי הם חלבונים רעים. ויכולים לגרום לפעילות אנזימטית לא רצויה ולצברי חלבונים פגומים בחלל התא ובממברנה. צבירים אלה נקראים אגרגטים (aggregates) [מקור1, מקור2, מקור3].
"נדהמנו לגלות שלחץ על התא למעשה חיסל את האגרגטים (aggregates) – לא על ידי השפלתם או ניקוים החוצה, אלא על ידי פירוק האגרגטים, מה שעלול לאפשר להם להתקפל מחדש בצורה נכונה", הסביר ראש המחקר אדוארד אוזוב, דוקטור. לחץ נחשף כאן כבעל יכולת ריפוי אלא שלא ברור עדין מה מידת הלחץ הרפואית במקרה ה"אם נוכל למצוא דרך להעיר את המנגנון הזה מבלי להלחיץ את התאים – מה שעלול לגרום ליותר נזק מתועלת – אז אולי נוכל למצוא דרך לטפל בכמה דמנציות."
–צ'פרונים מולקולריים (Molecular chaperones) הם חלבונים המסייעים לקיפול אלו חלבונים שמורים מאוד וכאמור מקדמים קיפול תקין של חלבונים אחרים in vivo (במציאות, כלומר לא במעבדה) [מקור]. מערכות מלוות מגוונות מסייעות בקיפול ותחלופה של חלבונים דה-נובו דוגמת הסלניום שהוזכר לעיל, אבל תוצר גוף לא כסלניום שמגיע מהמזון כתרופה (מתרחשות באופן ספונטני סמוך להפריה או במהלכה, כלומר לא עוברות בתורשה), כולל בהרכבה של קומפלקסים אוליגומריים והתאוששות מהתפשטות הנגרמת על ידי מתח.
רוב הצ'פרונים הם חלבוני הלם חום (HSPs).
הם אחראים על שיפוץ חלבונים והתאמות שגויות. תפקיד בסיסי של צ'פרונים מולקולריים הוא לעכב אינטראקציות חלבון לא יעילות. על ידי זיהוי והגנה על משטחים הידרופוביים שנחשפים במהלך הקיפול או בעקבות לחץ פרוטאוטוקסי, כנראה באיור למטה. הם יכולים גם להאיץ את תגובות הקיפול באופן תלוי ATP. עבודה אחרונה שקידמה את ההבנה שלנו כיצד הצ’פרונים פועלים כזרזים של קיפול חלבון החלה לאור ניסויים חלוציים של אנפינסן בשנות ה-50 [מקור] אלו הוכיחו שחלבון קטן יכול להתקפל באופן ספונטני בהיעדר גורמים נוספים במבחנה. (איור למטה). אבל מנגנון מאחד לקיפול חלבון נותר בלתי ידוע [מקור].
קיפול חלבון הוא תהליך רגיל בגוף, ובקרב אנשים בריאים התאים מבצעים סוג של בקרת איכות כדי להבטיח שהחלבונים מתקפלים בצורה נכונה ושחלבונים שלא מקופלים מושמדים.
[מקור].
למרות נוכחותן של מערכות המלווה, כמה שגיאות מתרחשות במהלך הקיפול וגורמי לחץ רבים כגון חום, יוני מתכות כבדות, רדיקלי חמצן ומוטציות עלולים לעכב את הקיפול הנכון.
[מקור1, מקור2, מקור3, מקור4, מקור5]
מספר גורמים מסבכים את תהליך הקיפול. ריכוזי כימיקלים שונים מקשים על קיפול חלבונים. כך, לדוגמה, ככל שריכוזו של כימיקל מסוים גדול יותר, החלבון נוטה לבחור בנתיב ארוך ו"מייגע" יותר מה שמאפשר לו להתמודדות עם יותר קשיים. בריכוזים נמוכים יותר של החומר, החלבון בוחר בנתיב קצר בהרבה, בו הוא יכול להשתמש בקיצורי דרך שחוסכים חלק מצורות הביניים, ובכל זאת מובילים אותו למבנה הסופי הנכון [מקור]. חלבונים "קשים" לקיפול הם בדרך כלל חלבונים גדולים מהממוצע ויש להם טופולוגיות מורכבות של קיפול. מסיבות אלו, הם זקוקים לאינטראקציה חזקה עם הצ'פרונים וגם עם הקוצ'פרונים, כך נוצרת רשת מקושרת הנקראת "צ'פרום" (chaperome) [מקור]. קבוצת החלבונים ה"קשים" אינה מסוגלת להשלים את הקיפול בצורה נכונה לבדה והיא זקוקה לצ'פרונים מיוחדים לביצוע משימת הקיפול, כמו HSP90s או הצ'פרונינים (chaperonins), כדי להשיג את המבנה הנכון [מקור]. מצב האנרגיה (מסומן בחץ שחור באיור למעלה מצד שמאל) משפיע אף הוא, שרשראות חלבון אשר נדרשות לעבור מחסומי אנרגיה משמעותיים בדרכן אל היעד, מתמודדות עם קשיים שכתוצאה מהם הן מאכלסות תוצרי ביניים מתקפלים (איור למעלה – או כאן). תוצרי ביניים אלו נמצאים מחוץ למסלול והופכים למלכודות קינטיות. קיפול איטי, ואינטראקציות תוך-מולקולריות שאינן מקוריות אך עלולות אף הן להוביל למצבים מתקפלים שגויים [מקור]. יתרה מכך, חומרי ביניים מתקפלים חושפים משטחים הידרופוביים שיכולים לעסוק באינטראקציות בין-מולקולריות לא פונקציונליות המאפשרות צבירה (איור למעלה). מחקרים ביו-פיזיקליים של קיפול חלבונים מתמקדים בדרך כלל בחלבוני מודל קטנים (לעתים קרובות < 100 חומצות אמינו) אלו מוגדרים למעלה קלים לקיפול, וקל לבטא אותם באופן רקומביננטי. הם גם שבים ומראים קיפול הפיך במבחנה [מקור1, מקור2, מקור3]. האתגרים הפנימיים הקשורים לקיפול של החלבונים בהחלט גדולים ומורכבים יותר מבחינה מבנית הם שמהווים את רוב הפרוטאומים (proteomes מונח המתאר את כלל החלבונים המתבטאים בגנום, בתא, ברקמה או באורגניזם השלם. השם הוא שילוב של המילים "פרוטאין" ו"גנום".) [מקור] עשויים להיות בולטים יותר ממה שמציעים מודלים קיפולים נוכחיים במציאות, כאשר קיפול שגוי הוא הכלל ולא היוצא מן הכלל. נראה שבעיית הקיפול הולכת וגוברת ואף מחמירה בתנאים in vivo. הריכוז הגבוה של מקרומולקולות בתא מפריע למהלך ומגביר את הנטייה של חלבונים לא מקומיים להצטבר [מקור], בעוד שלחץ פרוטאוטוקסי (proteotoxic stress) מערער את המצב הילידי. ידוע היטב שלחץ פרוטאוטוקסי משפיע על המסלול המיטוכונדריאלי של הפעלת קספאז (האיור למטה מתאר. זאת) [מקור] לחץ זה מעורר מוות של תאים – אפופטוטיים. הרמות המוגברות של הביטוי, הלכידה בתחום הממברנה המסוימת והשפעתו על הפתיחה של חלבונים מקופלים בצורה שגויה, ככל שאינה מובנת עדיין, מסייעת בפינוים [מקור1, מקור2, מקור3]. האיור למטה מתאר תהליך אפופטוטיי של גושי חלבונים רעילים כפי שמבינים אותו החוקרים כיום.
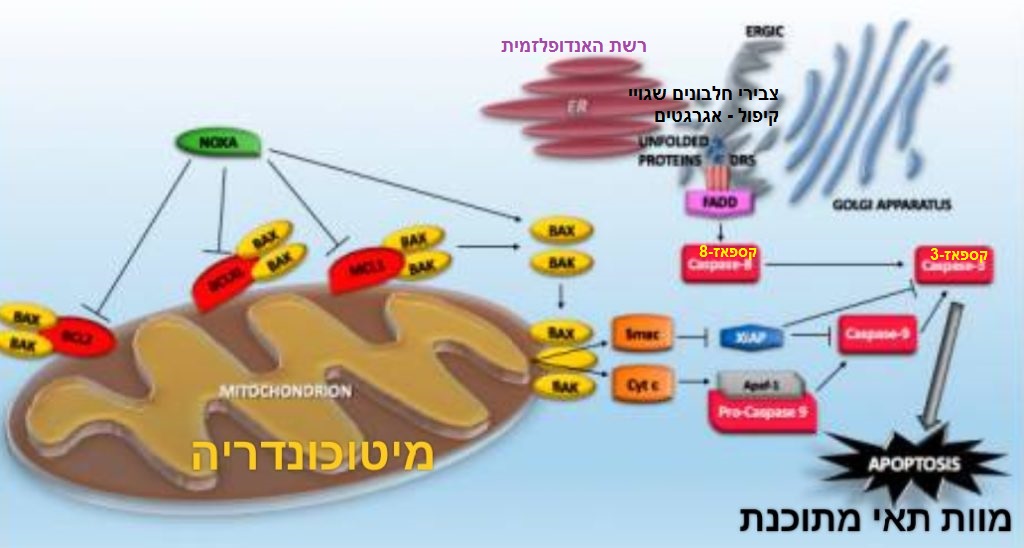
יתרה מכך, קיפול חלבון מתרחש בהקשר של תרגום [מקור], ופוליפפטידים בהתהוות כתוצאה מכך נחשפים לסביבה התאית במצב של חוסר מידע מבני הדרוש לקיפול יציב [מקור1, מקור2]. בתגובה לאתגרים הללו נוצרו צ'פרונים מולקולריים. הם שמלווים את התהליך ומסייעים לתקינותו. התפתחותם אפשרה למגוון הפרוטאומים גם בפרוקריוטים וגם באוקריוטים [מקור1, מקור2]. צ'פרונים משתמשים בווריאציות של מנגנון פעולה נפוץ המבוסס על קישור חולף של רצפים מועשרים בשאריות הידרופוביות. פעילות זו משמשת לעיכוב צבירה, אך יכולה גם להשפיע על האינטראקציות התוך מולקולריות המגדירות את מסלול הקיפול של חלבון. מחקר אחרון קידם את הרעיון שמלווה מולקולריות יכול לווסת נופי אנרגיה מתקפלים.
"כדי להימנע מהצטברות של אגרגטים ציטוטוקסיים, האברונים הביוסינתטיים (כלומר, הציטופלזמה, הרשת האנדופלזמית או ER, ומיטוכונדריה) פיתחו רשת פרוטאוסטזיס רב-שכבתית (PN) שמסייעת לחלבונים בהתהוות ומצילה או ממחזרת חומרי ביניים שגויים".
[מקור].
"נדהמנו לגלות שלחץ (שהופעל במעבדה) על התא למעשה חיסל את האגרגטים – החוקרים ציפו לכך שהלחץ יעודד שגיאות קיפול חלבון. אבל הלחץ חיסל את גושי החלבון הרעיל. לא על ידי השפלתם או ניקוים, אלא על ידי פירוק האגרגטים, מדובר באפשרות חדשה – והיא לאפשר לחלבונים להתקפל מחדש בצורה נכונה", הסביר ראש המחקר אדוארד אוזוב (Dr Edward Avezov). אוזוב ועמיתיו דיווחו על הממצאים שלהם ב-Nature Communications, במאמר שכותרתו, "התפרקות חלבון הנגרמת על ידי סטרס ברשת האנדופלזמית המזרזת על ידי BiP." [מקור]. UK Dementia Research Institute, University of Cambridge . פרופ' אוזוב ועמיתיו שיערו שהלחצת הרשת האנדופלזמית ה-ER שמתוארת באיור למעלה, עלולה להוביל לקיפול השגוי של החלבון ולהצטברותו ובהמשך גם להפחתת יכולתו לתפקד כראוי, מה שמוביל להצטברות מוגברת ולתחלואה הכרונית שנזכרה לעיל.
החוקרים גילו שהלחץ הוביל למסקנה מפתיעה ואחרת לגמרי – במקום להגביר את הקיפול השגוי, כמויות מסוימות של מתח סטרס, כנראה באיור למעלה, עלולות לגרום להסתלקות אגרגטים של חלבון.
כפי שאנו נלחצים מעומס עבודה כבד, כך גם תאים יכולים להילחץ אם הם נקראים לייצר כמות גדולה של חלבונים. למשל כאשר הם מייצרים נוגדנים בתגובה לזיהום. במחקר שנערך לאחרונה, חוקרים גילו שלחלבון הלם חום סיסטולי Hsp70 chaperone ולמערכת המסייעת שלו יש את היכולת לתקן שגיאות קיפול. הם יכולים לפתור הצטברות חלבון בציטופלזמה של התא, החומר בתוך התא ללא הגרעין. צ'פרונים ממחלקת Hsp70 (DnaK בחיידקים) הם מכונות מולקולריות אלוסטריות ביותר המשתתפות במגוון תהליכים תאיים, כולל קיפול וקיפול חלבון מחדש, טרנסלוקציה, פירוק ופירוק – ראו איור בקישור – כאן [מקור1, מקור2, מקור3].
פרופסור טארה ספירס-ג'ונס, Professor Tara Spires-Jones סגנית מנהלת המרכז למדעי המוח של גילוי באוניברסיטת אדינבורו, שלא היתה מעורבת במחקר, הוסיפה פרטים כשסיפרה ל-Medical News Today [מקור], כי הלחץ גרם להפעלה של חלבון מלווה או שהלחץ הזה 'עוזר' ומה שיכול לעזור לחלבונים אחרים להתקפל מחדש לצורות הבריאות שלהם במקום לערום גושים רעילים" [מקור], היא הוסיפה. המחקר פורסם ב- Nature.
"בנוסף על הידוע לנו כי אגוזי ברזיל (הסלניום אשר מופיע בהם בצורת סלנו-מתיונין (selenomethionine) מתקן חלבונים מקולקלים, התפרסמו לאחרונה כמה מחקרים על אנשים במדינות סקנדינביה" שתחלואת האלצהיימר בהם הייתה נמוכה מהמקובל, מסביר פרופ' אוזוב ומוסיף שהמחקר היה "על משתמשים בקביעות בסאונות. אוזוב מצביע על כך שהסאונה עשוייה להיות גורם משפר ומה שעלול להוריד את הסיכון לפתח דמנציה. הסבר אפשרי לכך לדעתו, הוא שמתח קל זה שנוצר ע"י החום הוא הסטרס המבוקש, והגורם לפעילות גבוהה יותר של HSPs, אשר עוזר לתקן חלבונים רעילים."
נשארו לך שאלות
אשמח להשיב על כל שאלה
לטופס פנייה ישירה אל ירון מרגולין – נא להקליק – כאן
בבקשה לא להתקשר משום שזה פשוט לא מאפשר לי לעבוד – אנא השתמשו באמצעים שלפניכם –
למען הסר ספק, חובת התייעצות עם רופא (המכיר לפרטים את מצבו הבריאותי הכללי של כל מטופל או שלך) לפני שימוש בכל תכשיר, מאכל, תמצית או ביצוע כל תרגיל. ירון מרגולין הוא רקדן ומבית המחול שלו בירושלים פרצה התורה כאשר נחשפה שיטת המחול שלו כבעלת יכולת מדהימה, באמצע שנות ה – 80 לרפא סרטן. המידע באתר של ירון מרגולין או באתר "לחיצות ההחלמה" (בפיסבוק או MARGOLINMETHOD.COM ), במאמר הנ"ל ובמאמרים של ירון מרגולין הם חומר למחשבה – פילוסופיה לא המלצה ולא הנחייה לציבור להשתמש או לחדול מלהשתמש בתרופות – אין במידע באתר זה או בכל אחד מהמאמרים תחליף להיוועצות עם מומחה מוכר המכיר לפרטים את מצבו הבריאותי הכללי שלך ושל משפחתך. מומלץ תמיד להתייעץ עם רופא מוסמך או רוקח בכל הנוגע בכאב, הרגשה רעה או למטרות ואופן השימוש, במזונות, משחות, תמציות ואפילו בתרגילים, או בתכשירים אחרים שנזכרים כאן.
מאמרים אחרונים
- סטרס יכול לעתים גם לרפא – מחקר חדש על תאי המוח
- רככת היפופוספטמית (זרחן נמוך מהנורמה) – מחלת כליות כרונית – או הפרעת עצם מינרלית
- מחלת כליות פוליציסטית אוטוזומלית דומיננטית (ADPKD)
- גמילה מאלכוהול – תהליך קשה, תסמינים איומים
- הגל החדש של בדיקות דם בהחלט רוצה לייעל את הביצועים הספורטיביים שלך, לשפר את הרווחה הכללית ולהרחיב או להאריך את תוחלת החיים גם לסייע להחלמתך ללא תרופות ממחלות כרוניות
- רככת היפופוספטמית (זרחן נמוך מהנורמה) – מחלת כליות כרונית – או הפרעת עצם מינרלית
- סטרס יכול לעתים גם לרפא – מחקר חדש על תאי המוח
- מחלת כליות פוליציסטית אוטוזומלית דומיננטית (ADPKD)
- גמילה מאלכוהול – תהליך קשה, תסמינים איומים
- הגל החדש של בדיקות דם בהחלט רוצה לייעל את הביצועים הספורטיביים שלך, לשפר את הרווחה הכללית ולהרחיב או להאריך את תוחלת החיים גם לסייע להחלמתך ללא תרופות ממחלות כרוניות
- מדללי דם טבעיים – חומרים אנטי-תרומבוטיים: נאטוקינאז, ויטמין E, פלפל קאיין, כורכום, קינמון, וספורט מאפשרים טיפול בנוזלי הדם ללא תרופות.
- סלניום Se התגלה כאנטי- אייג'ינג ומגן מפני מחלות כרוניות
- מהו אימון שלפוחית השתן?
- פסוריאזיס, האם הימנעות מגלוטן מסייעת לחולי הפסוריאזיס
- מדללי דם טבעיים – חומרים אנטי-תרומבוטיים: נאטוקינאז, ויטמין E, פלפל קאיין, כורכום, קינמון, וספורט מאפשרים טיפול בנוזלי הדם ללא תרופות.
- מחלת כליות פוליציסטית אוטוזומלית דומיננטית (ADPKD
- אי ספיקת כליות – הגורמים השכיחים ביותר ל-CKD הם סוכרת שנשלטת על ידי תרופות = שליטה גרועה בסוכרת ויתר לחץ דם שמטופל לכאורה על-ידי תרופות
- רעלים אורמיים מקדמים דיאליזה – הוכח לאחרונה שרעלנים אורמיים קשורים למיקרוביוטה של המעי הגס – איך להחלים ללא תרופות ולהימנע מדיאליזה.
- רככת היפופוספטמית (זרחן נמוך מהנורמה) – מחלת כליות כרונית – או הפרעת עצם מינרלית.
- גודש נוזלים בריאות – בקרב חולי כליה
- דלקת כליות אינטרסטיציאלית – השתמשו במי שעורה
- יתר לחץ דם – שינוי פרדיגמה וגישות חדשות – לחץ דם גבוה וטיפול טבעי ללא תרופות לאחר שטיפול תרופתי נערץ כשל
- הומוציסטאין, ויטמינים ומניעת מחלות כלי דם
- פרפור פרוזדורים (A-fib) יכול להפסיק מעצמו.
- טיפול בכאב עם אופיואידים גורר אותך לצרות צרורות למשל עצירות איומה. מה לעשות?
- גאוט הוא לא רק יתר פורין – החיים עם גאוט תלוי גיל ומין – האם אפשר לנצח גאוט בלי לבלוע הורמוני מין?
- גמילה מאלכוהול – תהליך קשה, תסמינים איומים
- רוצה להחלים בצורה פשוטה ביותר, ללא תרופות ממחסור בטסטוסטרון או מירידה במדד ה SHBG ?
- אי ספיקת כליות – טיפול ללא תרופות
- על ההשפעה האיומה של חלבון מן החי על הכליות
- אילוף הכליות הסוררות
- גודש נוזלים בריאות – בקרב חולי כליה
- עשרת המזונות הבריאים ביותר לחולי כלייה – קמח קליפת רימונים (PPF) .9
- הגיל השלישי, תאוותיה של הזיקנה – ואיך להתבגר יפה, טוב ובריא
- סלניום Se התגלה כאנטי- אייג'ינג ומגן מפני מחלות כרוניות
- מהו אימון שלפוחית השתן?
- פסוריאזיס, האם הימנעות מגלוטן מסייעת לחולי הפסוריאזיס
- מסלול ההתפתחות הנורמטיבי בחיי אדם ודמימותיו בטבלה. עמוד 18
- מסלול ההתפתחות הנורמטיבי בחיי אדם ודמימותיו בטבלה. עמוד 17
- מסלול ההתפתחות הנורמטיבי בחיי אדם ודמימותיו בטבלה. עמוד 16
- מסלול ההתפתחות הנורמטיבי בחיי אדם ודמימותיו בטבלה. עמוד 15
- מסלול ההתפתחות הנורמטיבי בחיי אדם ודמימותיו בטבלה. עמוד 14
- רעלים אורמיים מקדמים דיאליזה – הוכח לאחרונה שרעלנים אורמיים קשורים למיקרוביוטה של המעי הגס – איך להחלים ללא תרופות ולהימנע מדיאליזה
- ציר המעיים-מוח פסיכוביוטיקה psychobiotics
- אוכלוסיית המעי הגס חיידקים טובים, דיסביוזיס ו "שומר הגנום" גן p53
- גאוט הוא לא רק יתר פורין – החיים עם גאוט תלוי גיל ומין – האם אפשר לנצח גאוט בלי לבלוע הורמוני מין?
- אומגה 3 צמחית (שמן חרדל, שמן מרווה מרושתת) עולה על צורות אחרות של אומגה 3 ויש והן לבדן תורמות לבריאות בעוד האחרות עלולות להזיק יותר משלהועיל לך
- התכנית לשיקום הכליות פרק ז' – עקרונות הטיפול
- התכנית לשיקום הכליות פרק ו' – התבוננו אל מדד האוראה
- התכנית לשיקום הכליות פרק ה' תנגודת לאינסולין
- התכנית לשיקום הכליות פרק ד'
- התכנית לשיקום הכליות פרק ג
- התכנית לשיקום הכליות פרק ב
- התכנית לשיקום הכליות – פרק א'
- קריאת הגוף – מה אומרות פניך
- גלוטתיון כל האמת
- סיבו Sibo צמיחת יתר של חיידקי המעי הדק
- חומצה אלפא לינולנית משפרת את תוחלת החיים – צריכה גבוהה של חומצות שומן מצמחים נחשפה כגורם שמאריך את החיים.
- תובנות חדשות אי-ספיקת כליות תלויה במצבו של ציר FGF23-Klotho
- Tsamba שתי כוסות גרגרי שעורה דגנים מלאים, רצוי אורגניים – מתכון צ'מפה למבקשים להחלים מאי ספיקת כליות
- פאראצטמול (PARACETAMOL) גם פרצטמול או אצטאמינופן (Acetaminophen) – הידוע גם בשם אקמול, רוקסט ודקסמול עלול לפגוע בכליות ובכבד ואסור לשימוש לחולי כליה
- מקצבים בעולם החי – שעון ביולוגי בתאי הגוף
- מזון למוח – המזון הבריא למוח תומך בגמישות מערכת העצבים שלו וביכולת הלמידה, שומר על הזכרון, ומונע מחלות כגון אלצהיימר.
- מרחבי חיים מאריכי חיים – האזורי הכחולים
- קשר הגלוטן – אלרגיה לגלוטן והאם הימנעות מגלוטן מוצדקת?
- מהן עיניים אדומות?
- האם תוסף ויטמין D בולם את מחלת הכליות בקרב סוכרתיים?
- גלוטמין (Gln) -המגן הגדול על בריאות האדם – כל מה שחשוב לדעת
- פיקנוגנול – כל האמת על רפואת עץ האורן והכנת התה ממחטיו
- תחמוצת החנקן (NO) כיווץ תאי האנדותל, מחלות כרוניות קשות – ודרכי ריפוי חדשות
- מחשבון מדידה והערכת קצב הסינון הגלומרולרי (GFR) אשר מבוסס על קריאטינין, נתוני גוף, גיל, גזע ומין.
- הגיל השלישי, תאוותיה של הזיקנה – ואיך להתבגר יפה, טוב ובריא
- בני-על – האם יש גבול ביולוגי למספר השנים שאדם יכול לחיות?
- לראשונה, מדענים הצליחו לתרגם לטקסט את הפעילות המוחית של אדם עם שיתוק שאינו מסוגל לדבר.
- רוצה להחלים בצורה פשוטה ביותר, ללא תרופות ממחסור בטסטוסטרון או מירידה במדד ה SHBG ?
- טיפולים מבוססי רירית לזיהומים נגיפיים וחיידקיים
- מחסור בברזל
- פיקנוגנול – כל האמת על רפואת עץ האורן והכנת התה ממחטיו
- סגולותיהם של זרעי החרדל
- דרכים חדשות לוויסות יעיל של טריגליצרידים (Triacylglycerols) בדם
- שוויון בריאותי?
- טיפולים מבוססי רירית לזיהומים נגיפיים וחיידקיים
- מה הם בקע (קִילֶה) חתך, מדוע הם מתרחשים ומה לעשות?
- קרום התא – הממברנה והדלקת הכרונית
- עשרת המזונות הבריאים ביותר לחולי כלייה על האצות והפוקוקסנטין, חלק 7.
- האם תזונה נוגדת דלקת יכולה לעזור?
- חידושים ומהפכות בנושא יתר לחץ דם.
- נוגדני ANF – גורם אנטי גרעיני ונוגדן אנטי-ציטופלזמי של נויטרופיל – ANCA
- תעוקת חזה מיקרו-וסקולרית
- "מגיפת המאה העשרים ואחת", מיתוסים רפואיים: כל מה שחשוב לדעת על אלרגיות
- דרכים חדשות לוויסות יעיל של טריגליצרידים (Triacylglycerols) בדם
- מזון כתרופה
- חומציותו של הנוזל הבין תאי בגוף האדם מונעת תהליכי החלמה במחלות כרוניות קשות – מה לעשות?
- אנטיביוטיקה – על נזקיה לאנשים בכלל ובפרט לחולים
- חומץ אננס – רוצה לדעת כיצד להכין תרופה ביתית, אנטי-דלקתי מקליפות האננס?
- חומצה אורית Uric acid צום פורינים – מצב המכונה גם היפראוריקמיה וטופי.
- זרחן – Phosphorous, והאם מוכרחים להתחיל בדיאליזה טרם נבחנה רמתו של גורם צמיחה פיברובלסט 23
- עשרת המזונות הבריאים ביותר לחולי כלייה על האצות והפוקוקסנטין, חלק 7.
- שלושת המיצים
- לסדרת מאמרי – מבוא לתורת הגוף-נפש המודרנית – חלק א
- על הכאב בברך שמקשה לעלות במדרגות ומה שעומד מאחריו
- להתסיס שיבולת שועל – מתכון וכל הסודות.
- כל מה שאתה צריך לדעת על מיקרו-תזונה – ויטמינים ומינרלים
- למה מדידת הויטמין B12, רחוקה מלהיות מדויקת?
- ירקות ירוקי עלים לרוב טובים לבריאותנו, לפעמים הם לא – רוצה לדעת מתי כדאי לצרוך עלים ירוקים?
- תרופות ללחץ דם גבוהה נמצאו כקשורות לסיכון מוגבר לסכיזופרניה
- תרופה ישראלית חדשה לקורונה
- מזון כתרופה – שמן זית ושמן קנולה או חרדל הצילו מאות ילדים בעולם.
- מזון כתרופה – אפשר להחלים מאי ספיקת כליות
- עשרת המזונות הבריאים ביותר לחולי כלייה – על השעורה (דגן) ופעולות נוגדות דלקת כולל עיכוב גורם נמק גידול אלפא – Tumor necrosis factor alpha (TNF-α).
- האסכולה הונציאנית (ציור) חלק א' מאת ירון מרגולין
- איך להיראות צעיר מגילך – כל הסודות
- Reconstruction of erythropoietin by the kidneys without drugs
- קטואנאלוג ketoanalogue
- תרופות ללחץ דם גבוהה נמצאו כקשורות לסיכון מוגבר לסכיזופרניה
- חומץ אננס – רוצה לדעת כיצד להכין תרופה ביתית, אנטי-דלקתי מקליפות האננס?
- תככים ומזימות – האמת סביב גירוש יהודי ספרד – 1
- כתף ימין וסופו הטראגי של מבצע גאוני – פייר-פול ריקה
- משחה צהובה – לכאבי שרירים – משחת הפלא להפחתת כאבים
- על הנקמה – פנטזיות נקמה לאחר חווית אירועים טראומטיים
- פרנצ'סקו מסינה Francesco Messina אלהים באדם שחיפש אחר היופי
- פייר בושאן – האיש שהציל את חגיגת הנישואין של לואי ה-14 מאת ירון מרגולין

כתיבת תגובה