הומאוסטזיס של האנרגיה בגוף האדם
התאוריה העדכנית ביותר רואה ב EI (צריכת אנרגיה) ובהוצאתה כמי שנשלטת למעשה מתוך שיקולי עומק של ויסות משקל הגוף, ובמיוחד, ויסות של מסת השומן של הגוף [מקור1, מקור2, מקור3]. (FM), לפטין הוא הורמון שמופק מרקמת השומן ועומד במרכז התיאומים והאחריות על ושל הויסות הזה. בעקבות גישה זו רקמת השומן, החלה לעורר עניין מחודש. איזון רקמת השומן, שמירה על יציבותה של רמסת השומן הם המניעים העיקריים כנראה של צריכת המזון היומיומית של מזון [מקור1, מקור2, מקור3, מקור4, מקור5, מקור6].
Energy Metabolism and Appetite Control
רעב בבני אדם, כבאורגניזמים אחרים, הוא צורך פיזיולוגי המערב מערכות ביולוגיות כגון מעגלי מוח עצביים, הורמונים ומערכות איברים [מקור].
המאמר יעמוד על תפקידם של מתווכים מערכתיים כגון לפטין וגרלין, בוויסות ההומיאוסטטי של האכלה. לפטין וגרלין, פועלים על מערכות מוח המשתמשות בנוירופפטיד Y, פפטיד הקשור לאגוטי, מלנוקורטינים, אורקסינים וההורמון מלנין. גם המנגנונים המשפיעים של מערכות טעם ותגמול המספקות למזון את תכונותיו המנחמות, ומחזקות באופן מהותי יוצגו הקשרים בין המערכות ההומיאוסטטיות וההדוניות שתיהן שולטות על צריכה של תזונה נאותה, מחלימה או מפריעה לתהליכי החלמה בקרב חולים כגון חולי כליה, לב, יתר לחץ דם, סוכרת ואלצהיימר.
ניתן להפריד את התנהגות האכילה להאכלה נהנתנית והאכלה הומאוסטטית. פרק זה מכיר בכך שאכילה יכולה להתרחש ללא רעב בתגובה לגורמים רגשיים וחברתיים, ויכולה להתרחב מעבר לשובע [מקור]. עם זאת, המוקד של פרק זה הוא על האכלה הומאוסטטית וכיצד הורמונים בגוף מייצרים רעב ושובע.
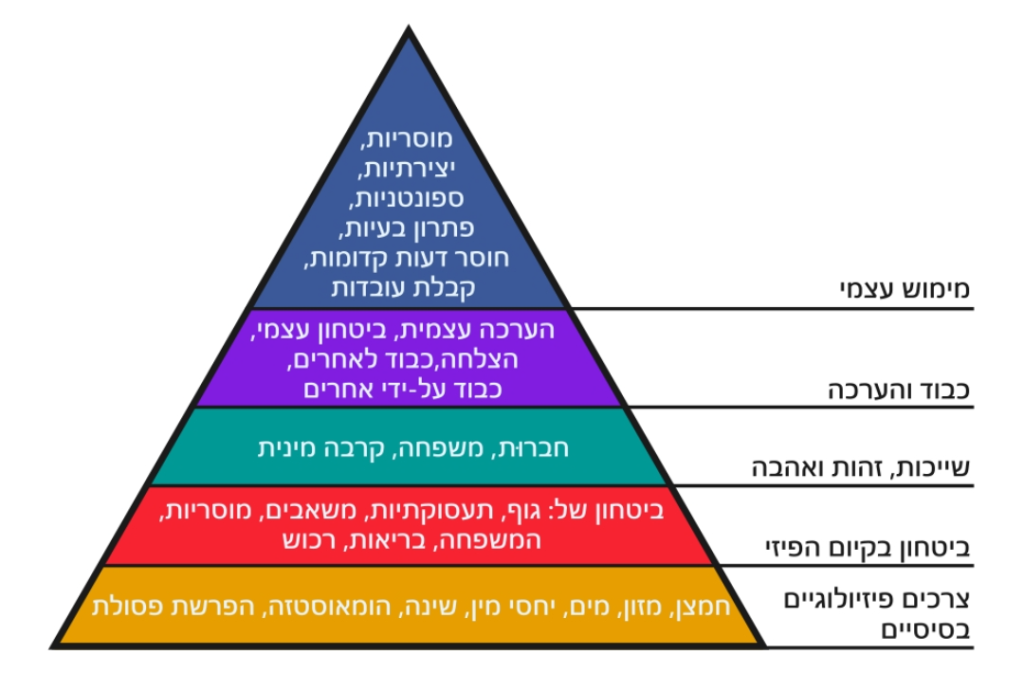
על פי תיאורית הצרכים של הפסיכולוג אברהם מאסלו (Abraham Maslow) והיררכיית הצרכים שלו, על 5 סטים של מטרות (צרכים בסיסיים) הקשורים זה לזה וחלקם מקבילים ומסודרים בהיררכיה. ניתן לסווג צרכי יסוד כצורך לגדול או לצמוח ולצרכי מחסור. במקרה של צרכים פיזיולוגיים, כמו רעב, אלו מסווגים כאן במדור לצורכי המחסור [מקור]. כאשר מתמלא הצורך הבסיסי – או כאשר המטרה הבולטת ביותר מתממשת, צץ ועומד באופק צורך חדש שנמצא בפירמידת הצרכים של מאסלו, כנראה באיור שמפרש אותה למעלה, גבוה יותר. "לכן האדם הוא ייצור שצריך תמיד וגם תמיד רוצה." הכל בסדר מבחינה פיזיולוגית עד שחוסר כלשהו מפעיל צורך בתוך האורגניזם לקיים אינטראקציה עם הסביבה כדי לתקן את החסר. מכאן שכאשר צורך פיזיולוגי אינו מסופק במשך זמן מה, הוא יוצר מצב מוטיבציוני השולט בתודעה [מקור1, מקור2, מקור3] (Maslow, 1943). איום או חיסול אפשרות לממש צורך, איום ממשי או קרוב, על צרכים בסיסיים כפי שהתרחש תחת הכיבוש הנאצי ולעתים גם במקומות אחרים מנהל חרדה ומספק תחושת איום קיומי שעלול להוביל לפסיכופתיה [מקור].
המנגנונים המרכזיים שהוגדרו בראשית שנות ה- 50, כמי ששולט על צריכת המזון שלנו הומשגו באותם ימים: "מרכזי רעב ושובע" [מקור1, מקור2, מקור3] מאז אלו עברו סדרה רצינית של שינויים, ואפילו שיפורים מתקדמים הנובעים מההתקדמות הטכנית במדעי המוח [מקור]. המאפיין עיקרי של האידיאה: "מרכזי רעב ושובע" סבב את רעיון ההומאוסטזיס וההקבלה שלו קיברנטיקה (cybernetics – חקר מערכות הבקרה ועקרונות המשוב בבני אדם) או בתורת הבקרה [מקור]. שתי העמדות הללו התמקדו באותות משוב שניטרו סטייה מסוימת מערך גופני אידיאלי כלומר, החלה של התאמות מפצות באמצעות בקר מרכזי. הרעיון של ויסות עמד במרכז תפיסה זו. האמירה: "כל תא בגוף תלוי בהורמוני בלוטת התריס לוויסות חילוף החומרים שלו וייצירת אנרגיה לתפקודו" נובעת ממנה. משקל הגוף נושא שיעמוד במרכז המאמר הזה עמד במרכז התמונה גם בתחילת הדרך אבל כמשתנה המוסדר על ידי "מרכזי רעב ושובע". רעיון הטרמוסטת כמו במרחבי השליטה בטמפרטורת הסביבה בחדר שמבוקר על ידי תרמוסטט הייתה למשל שנישא בפי כל דוגלי האסכולה: "מרכזי רעב ושובע". אכן, נראה שחלק מהמערכות הפיזיולוגיות פועלות בצורה זו, וההנחה היא שהויסות חל באותה מידה על הקשר בין השליטה בצריכת המזון לבין "ויסות" משקל הגוף. אם אכן מתרחשת ויסות אמיתי, המחקר סבב את השאלה האם המשתנה המווסת הוא משקל הגוף נטו, רקמת שומן שלו או מסה נטולת שומן (FFM). מכאן צמחו המושגים שחקרו את הרכב הגוף, ההוצאה האנרגטית שלו מול צריכת המזון שלנו [מקור]. בולטת בגישה זו תיאורטיות הגלוקוסטטית של מאייר כפי שפורסמה בשנת 1953 [מקור]. התיאוריה הגלוקוסטטית הניחה שצריכת המזון מתבצעת כדי לשמור על הרמות הנכונות של גלוקוז – סוכר בדם. תיאוריה זו מכונה גלוקוסטטיקה. כלומר, אנו אוכלים ע"פ תהנחה זאת כאשר רמות הגלוקוז בדם יורדות ומפסיקים לאכול לאחר שהערכים הרגילים משוחזרים [מקור]. יותר מאוחר החלנו להיחשף להשפעות המזיקות של סוכר על המוח.
כשתפריט התזונה שגוי, התרופה לא עובדת; כאשר המזון הוא תרופה, אין צורך בתרופות.
אנשים שנדחפים כמו מתוך איזה צורך פנימי לצרוך סוכר ובכמויות גדולות יותר כדי להרגיע את הצורך בסוכר. הסוכר משחרר כמות גדולה של אנדורפינים במוח (תחושת אושר, אשר אורח חיים ואירועים בחיינו אינם מעניקים לנו את אותה התענוג). מחקר שערכו חוקרים מאוניברסיטת קליפורניה על צריכת פרוקטוז (סוכר שנמצא בירקות, פירות ודבש) הראה כי לחומר זה יש השפעות שליליות על היווצרות סינפסות במוח. כלומר פרוקטוז פוגע ביכולת שלנו ללמוד וליצור קשרים חברתעיים חדשים. נמצא כי קיים מתאם בין צריכת סוכר להופעתה של מחלת האלצהיימר עד כדי מחשבה לסווגו כסוכרת מסוג 3. עודף סוכר שמקורו מתפריט סוכר רב משפיע גם על מצב הרוח. עודף סוכר, לאור ההשפעות על האינסולין בגוף, עלול לעורר תחושת דיכאון, וחרדה. הגלוקוז מזין את המוח, אבל בצריכתו, המוח משחרר סרוטונין, אחד ממוליכי העצבים המעורבים בתחושת ההנאה. מאגרי הסרוטונין אינם אינסופיים: מכיוון שהוא משתחרר ברציפות, פחות ופחות יישארו במוח. במהלך המח אדם שצורך עודף סוכר עלול להתקשות בחווי של רגשות חיוביים ברציפות. בנוסף הסוכר פועל על אוקסיטוצין – נוירוטרנסמיטר (מוליך עצבי) שמשדר שובע – בא להזהיר את הגוף שאנחנו שבעים ואין צורך לאכול יותר. הגלוקוז 'משבש' את מנגנון השובע ואנשים שאוכלים מתוק לא מרגישים שבעים גם אחרי פרוסת עוגה של 1500 קלוריות.
למאמרי על דרכי החלמה ממחלה האלצהיימר – כאן
למאמרי על דרכי החלמה מסוכרת – כאן
למאמרי על דרכי החלמה מאי ספיקת כליות – כאן.
קכקסיה – הרזון הקטלני של חולי כליות בדיאליזה – כאן.
הוויסות של צריכת האנרגיה הוא הבסיסי לכל המנגנונים ההומיאוסטטיים כותב מאייר בספרו (1953). ומאזכר את ארבע תיאוריות שבאו להסביר את תופעת הרעב מהמאה ה- 19: התיאוריות של מוצא פריפריאלי (האלר, ארסמוס דרווין, יוהנס מולר וובר) [peripheral origin (Haller, Erasmus Darwin, Johannes Müller and Weber)] קבעו כי תחושת הרעב נובעת מגירוי של כל העצבים האפרנטיים בעיקר ב- בֶּטֶן [מקור]. דברי פליני (הבמאי האיטלקי): 'החיים הם שילוב של פסטה וקסם.' מאזכרים את תחושת הרעב בבטן, אבל גם שרבים אוכלים להנאתם כי אוכל יכול גם להעניק רוגע, נחמה. מזונות מסוימים משקיטים געגועים לבית ילדותנו. נושא זה יחזור כשנתקדם לתיאוריות החדשות ביותר.
תיאוריית חומצות האמינו יצאה באמצע שנות ה-50 וגרסה כי הרעב והרצון לאכול נקשר בריכוזי החלבון בדם [מקור]. בשנת 1953 גם חומצות שומן חופשיות lipostatic theory שמשו את ההנחה של המנגנונים ההומיאוסטטיים זו התיאוריה הליפוסטטית. התיאוריה הליפוסטטית סוברת שלכל אחד מאיתנו מדד לשומן בגוף. גישה זו הניחה שהוויסות לטווח ארוך של צריכת המזון נשלט על ידי הריכוז בדם של חומצות שומן חופשיות. אלו נובעות מחילוף החומרים של שומן. ריכוזים גבוהים של שומן בדם מעידים על פירוק השומן, וצריכת המזון עולה בהתאם לנוכחותם; ריכוזים נמוכים קשורים להפחתה בצריכה של אוכל.
כיום מדברים על לפטין כמי ששולט על מנגנון הרעב. אדם רעב מחפש לאכול משהו.
לפטין הוא אות המעביר מידע מהפריפריה למוח בנוגע למצב ארוך הטווח של מאגרי האנרגיה בגוף [מקור]. בהתבסס על מחקרים מולקולריים בבעלי חיים ומבחנה במעבדה, כיום חושבים ששינויים בריכוזי הלפטין במחזור הדם משנים את הביטוי ההיפותלמי (אזור, במוח האדם, מכונה מוח רגשי) שם הוא נקלט ומגרה מולקולות
אֵפֶקְטוֹר או מודולטור, (מולקולה הנקשרת לחלבון אלוסטרי), סוגים של נוירופפטידים (מוליכים עצביים) כמו נוירופפטידים אנורקסיגניות ואורקסגניות, מוליכים שמעודדים תגובות מתקנות בצריכת אנרגיה (EI) והוצאה של אנרגיה, כדי למזער הפרעות באיזון האנרגיה [מקור1, מקור2.].
רוצה לומר שהנוירונים שבמוח שלנו מעבדים מידע מהגוף למשל מרקמת השומן המגיע באמצעות הורמונים כלפטין ושליחים כימיים אחרים אליהם, בשעה שהגוף זקוק לאנרגיה ומזון, כלומר רעב.
תקשורת לקויה היא פגע שנוצר בין תאי המוח, ומונעת ממנגנון השובע לפעול כיאות.
לפטין (ואדיפונקטין) הם הורמונים שמקורם ברקמת השומן והמעי הדק, בעיקר באנטרוציטים;
מקור זה שיכנע את החוקרים לראות ברקמת החיבור חלק מהמערכת הנוירואנדוקרינית. יצוין כי להבדיל מאדיפוקינים אחרים דוגמת לפטין, רמות אדיפונקטין בדם מצויות ביחס הפוך למסת רקמת השומן, כלומר ככל שמסת רקמת השומן בגוף גדולה, רמות האדיפונקטין בדם נמוכות יותר.
לפטין הוא הורמון שעוזר לווסת את מאזן האנרגיה על ידי הפעלת השפעה על ההיפותלמוס, בלוטת יותרת המוח ובסופו של דבר על דיכוי הרעב.
אדם לא רעב בדרך כלל לא אוכל וכתוצאה מכך מסת השומן בגופו מנוצלת לתחזוקת הגוף ומופחתת. הפחתתה מתרחשת באדיפוציטים (adipocytes – קבוצת התאים המצויים ברקמת החיבור ומרכיבים בעיקר את רקמת השומן, ומתמחים באגירת אנרגיה כשומן). ללפטין יש רצפטורים (קולטנים) ספציפיים בגרעינים הונטרומדיאליים (גרעיני הבסיס – גרעינים מכילים ריכוז של גופי תאים, ולכן מזוהים בחתך אנטומי כחומר אפור) ובגרעינים שבהיפותלמי הקשתי שבמוח הריגשי (היפותלמוס) ובחלקים אחרים של ההיפותלמוס גם במרכז ההזנה באזור הטגמנטלי הגחוני (אזור בטגמנטום של המוח האמצעי). רבים מהמבנים והאזורים המוכרים במוח שלנו כמו למשל: בתלמוס ובהיפותלמוס הם למעשה אוסף של גרעינים רבים המחוברים ביניהם, גרעיני הבסיס, (שהוזכרו הם דוגמא להם) והם ממלאים תפקידים רגולטוריים (מסדירים פעילויות) לא רק תאי שומן,. מנגנון מערכת השובע הוא כה מורכב, עד כי הסבירות לטעויות וליקויים בו גבוה מאוד, כך למשל גם חלק זה שבמוח, למשל הקולטנים של לפטין. הקולטנים של לפטין מקבלים את שעריו ומעביירים אותם הלאה אבל בהשמנת יתר, הם לכאורה לא קולטים ולא בולמים את האכילה, כך נקשרת השמנה לאובדן רגישות של קולטני לפטין, נושא זה נחקר כיום מוכר ומכונה תנגודת ללפטין, וכתוצאה מכך אנו עדים לחוסר יכולת לייצר שובע או דיכוי של הרעב, מה שגורם אחריו עלייה בצריכת המזון, קשיים אדירים באיזון כמויות וסוגי מאכלים והשמנה. בנוסף, ללפטין תפקיד בהנקה, בצפיפות העצם, במערכת החיסון, בטיפולי סוכרת והיפרטריגליצרידמיה, באיזון תפקודה של בלוטת התריס, בעייפות כרונית, בראד בידיים. המחקרים האחרונים בלפטין מצביעים על כך שאנלוגי של לפטין עשוי לטפל ב-DM והיפר-טריגליצרידמיה.
ההורמון לפטין מופרש כנזכר לעיל, מרקמת שומן ורמתו במתאם עם רמת השומן בגוף [מקור].
הלפטין מדווח להיפותלמוס (נושא שהוזכר למעלה) על מצבי שובע, ומפחית את התיאבון, וכתוצאה מכך יש ירידה בזלילה, באכילה או בצריכת הקלורית. במצבים של רעב, תת תזונה או אנורקסיה, רמות הלפטין נמוכות. באנשים בעלי עודף משקל, רמות הלפטין תהיינה גבוהות, אולם בגלל תנגודת ללפטין אשר מתרחשת כנראה בגלל ריוויון של הרצפטורים ללפטין בהיפותלמוס, הרעב ממשיך, גם האכילה והתאבון לא נבלם.
לפטין אינו מופרש מיד לאחר ארוחה, אלא עוברות מספר שעות עד שרמתו עולה משמעותית וניכרת בזרם הדם. הפרשת הורמון זה באדם היא פעימתית. משך הפעימה כחצי שעה. מערכות גוף שאף הן פעימתיות באופיין כמו ציר היפותלמוס-היפופיזה-אדרנל מווסתות על-ידי לפטין . ציר היפותלמוס בלוטת התריס, וכן הגונאדות. כלומר האיברים בהם מיוצרים, ולעיתים גם מאוחסנים, תאי הרבייה (הגמטות) מווסתות על-ידי הלפיטין. הגונדות אצל הזכרים הם האשכים והשחלות אצל הנקבות.
כתוצאה מרעב, בציר בלוטת התריס רמות של ההורמונים T4 ו-T3 יורדות. אחד התסמינים לכך הן בצקת היקפית (במבוגרים). פעמים רבות בצקות נובעות מצמא. מבוגרים רבים מונעים מעצמם מים, כדי לחסוך ריצות לבית שימוש, אבל מעטים מבחינים שהם למעשה בתת-תזונה ורעב. רמות T4 ו-T3 יורדות בדם בגלל רעב, מה שמוביל להיפותירואידיזם מרכזי central hypothyroidism כלומר לתת פעילות משנית של בלוטת התריס (היפופיזה – האונה הקידמית – באיור העליון מצוירת בירוק) מקור1, מקור2]. או תת פעילות של ההיפותלמוס (המוח השולט על המנצח הגדול בלוטת יוֹתֶרֶת הַמּוֹחַ Pituitary Gland) נושא שניכר בעייפות ובצקת היקפית (במבוגרים) [מקור]. דבר שנובע בבני אדם בעיקר מתפקוד לקוי של ההיפותלמוס ו/או בלוטת יותרת המוח [מקור]. נושא שמעמיד את ייסורי הנפש במרכז תמונה. כל השתבשות שהיא בבלוטת יותרת המוח לרוב היא תוצאה של מתחים נפשיים, מצבים מאתגרים, עצבים וחיים קשים עם סבל, בעיקר סבל רגשי וייסורי נפש שמקורו בחיק המשפחה, ניהול קריירה ומחלות כשהבולטת בהן לחץ דם גבוה מאד.
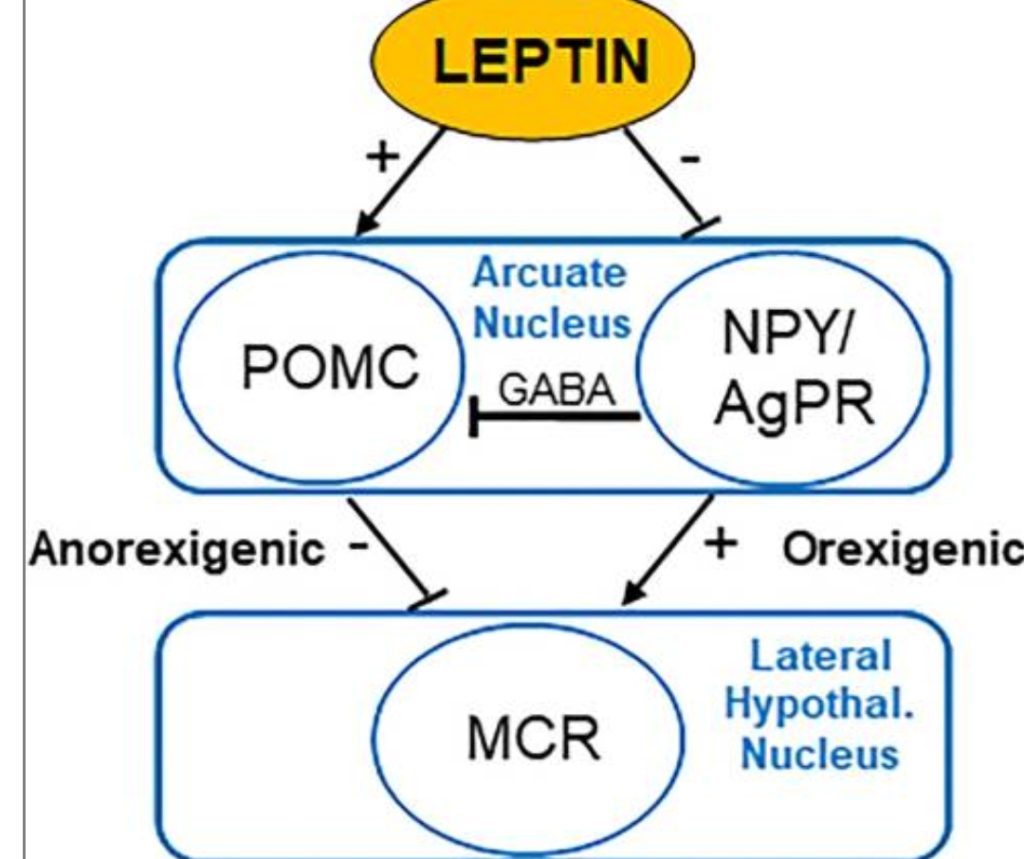
ההשפעה של לפטין על הומאוסטזיס האנרגטי שונה ממה שסברו החוקרים בתחילת הדרך. ההשפעה של לפטין היא א-סימטרית. כחצי שעה לאחר הארוחה לפטין מתחיל להיות מופרש. ירידה בלפטין במחזור הדם נחשבת כמעודדת צריכת אנרגיה energy intake (EI) – מפחיתה משקל [מקור]. זאת משום שצריכת אנרגיה (EI) או שריפת קלוריות מהווה את הבסיס של הפחתת משקל ומה שמכונה דיאטה, תוך שמירה על הזנה מלאה כך שכל שאר אבות המזון ההכרחיים לבריאות הגוף יסופקו. דיאטה נכונה חייבת להתבסס על תפריט הזנה שמספק בתוך התפריט המוצע את כל כמות המזון הדרושה גם כדי למלא את דרישת האנרגיה הבסיסית לתפקוד תאי הגוף. תנאי זה הוא אחד היותר רגישים בתהליכי החלמת הכליות. בתנאים של יציבות משקל, EI (צריכת אנרגיה) שווה להוצאת אנרגיה (EE – EI equals energy expenditure). רוצה לקרוא עוד על נושא זה בקישור הזה תמצא לך הסקירה המקיפה הראשונה של מחקרים שבהם דווח על EI ו-EE כפי שנמדדו באמצעות the doubly labeled water technique – כאן. אם נמשיך בנושא לפטין מופחת – הרי שהפחתה בלפטין קוראת ומעודדת את האדם לאכול ללא הגבלה. המוטיבציה לאכול מוגברת באמצעות ויסות מטה של הביטוי ההיפותלמי (המוחי) של נוירופפטידים אנורקסיגניים (anorexigenic neuropeptides) כגון פרואופיומלנוקורטין ( proopiomelanocortin – POMC) והורמון מגרה אלפא מלנוציטים (alpha melanocyte-stimulating hormone α-MSH) ווויסות עלייה בביטוי של נוירופפטידים אורקסיגניים כגון נוירופפטיד Y (NPY – neuropeptide Y) וחלבון קשור לאגוטי – (AgRP – agouti-related protein) [מקור] (AgRP) (Lenard and Berthoud 2008, Sainsbury and Zhang 2010) [מקור1, מקור2, מקור3, מקור4]. לפטין הולך ונתפס כמי שעומד מעל להיפותלמוס ושולט על הומאוסטזיס אנרגטי, כוכב חדש ומי שעומד במרכז התיאוריה הליפוסטטית של בקרת התיאבון the lipostatic theory of appetite control. בספר שיצא לאור בשנת 2017 :
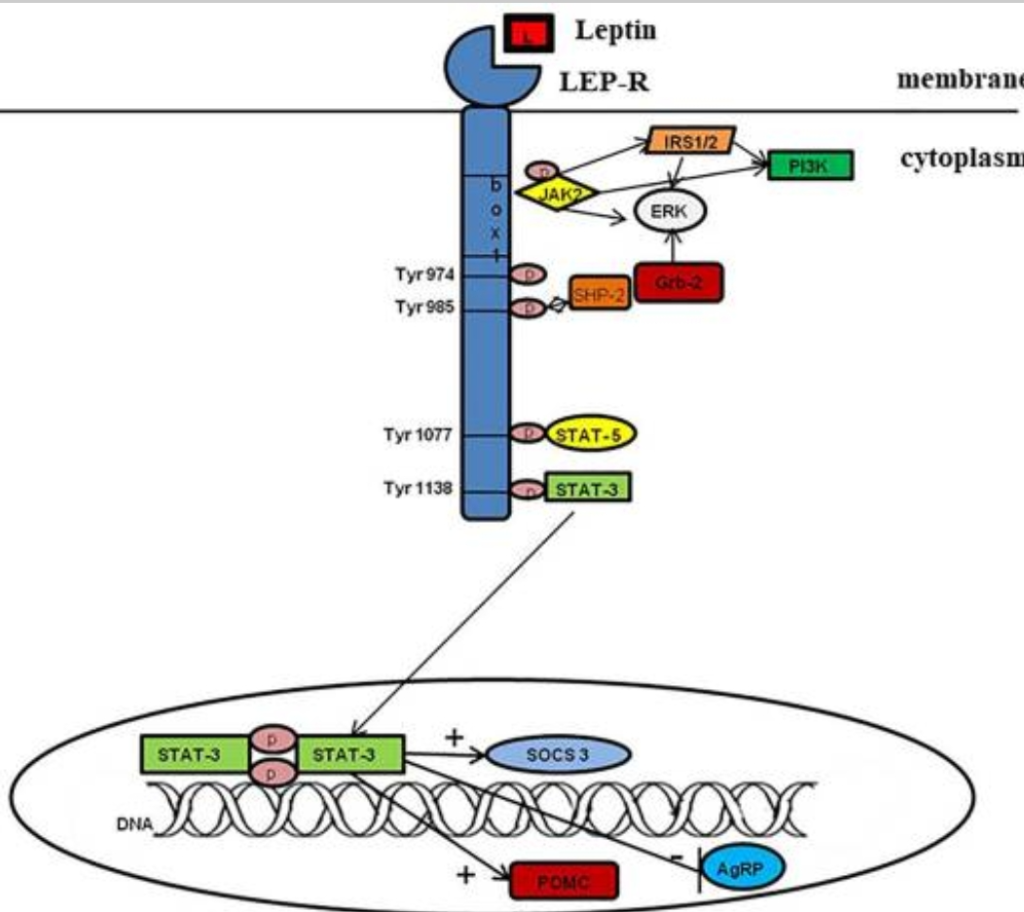
מקור האיור בצילום מסך מהמאמר:
Leptin and Obesity: Role and Clinical Implication – כאן
הפחתה בלפטין קוראת ומעודדת את האדם לאכול ללא הגבלה. המוטיבציה לאכול מוגברת באמצעות ויסות מטה של הביטוי ההיפותלמי (המוחי) של נוירופפטידים אנורקסיגניים (anorexigenic neuropeptides) כגון פרואופיומלנוקורטין ( proopiomelanocortin – POMC) והורמון מגרה אלפא מלנוציטים (alpha melanocyte-stimulating hormone α-MSH) ווויסות עלייה בביטוי של נוירופפטידים אורקסיגניים כגון נוירופפטיד Y (NPY – neuropeptide Y) וחלבון קשור לאגוטי – (AgRP – agouti-related protein) [מקור] (AgRP) (Lenard and Berthoud 2008, Sainsbury and Zhang 2010) [מקור1, מקור2, מקור3, מקור4]. לפטין הולך ונתפס כמי שעומד מעל להיפותלמוס ושולט על הומאוסטזיס אנרגטי, כוכב חדש ומי שעומד במרכז התאוריה הליפוסטטית של בקרת התיאבון the lipostatic theory of appetite control. בספר שיצא לאור בשנת 2017 :
כיצד גרלין (הורמון המגרה הפרשת הורמון גדילה, וכן משחק תפקיד מרכזי בויסות תיאבון ומשקל הגוף ) ולפטין משפיעים על הרעב והאכילה?
השמנת יתר היא ביסודה בעיה של איזון אנרגטי בכך שברור מאליו היא יכולה להתפתח רק כאשר צריכת האנרגיה עולה על ההוצאה האנרגטית [מקור].
How do ghrelin and leptin affect hunger and eating?
נבחן האופן שבו גרלין ולפטין משפיעים על הרעב ועל האכילה ותחושת השובע. כמו כן מוצגות תיאוריית השליטה הכפולה (the Dual-Control theory), התיאוריה הגלוקוסטטית, התיאוריה הליפוסטטית. אם נישאר בטווחי הליפטין
התאוריה העדכנית ביותר רואה ב EI (צריכת אנרגיה) ובהוצאתה כמי שנשלטת למעשה מתוך אינטרסים של ויסות משקל הגוף, ובמיוחד, ויסות של מסת השומן [מקור1, מקור2, מקור3]. (FM), לפטין הוא שעומד במרכז התיאומים של הוויסות הזה. בעקבות גישה זו רקמת השומן, איזון רקמת השומן שמירה על יציבותה של רמסת השומן הם המניע העיקרי של צריכת המזון היומיומית [מקור1, מקור2, מקור3, מקור4, מקור5, מקור6].
רקמת השומן יכולה להגיב במהירות למצבי חסר או עודף תזונתיים על ידי היפרטרופיה או היפרפלזיה של תאי השומן, ובכך למלא את יעודה בשמירה על שיווי המשקל האנרגטי של הגוף.
רקמת השומן
רקמת שומן מוכרת לנו בדרך כלל כשומן גופני. שומן כזה נמצא בכל הגוף. ניתן למצוא אותו מתחת לעור (שומן תת עורי), ארוז סביב איברים פנימיים ומגן עליהם (שומן קרביים), בין השרירים, בתוך מח העצם וברקמת השד. גברים נוטים לאגור יותר שומן קרביים (שומן סביב האיברים הפנימיים שלהם), מה שמוביל להשמנה סביב אמצע הבטן (שומן בטני [מקור]). נשים נוטות לאגור יותר שומן תת עורי בתוך הישבן והירכיים (השמנת אגס). הבדלים אלו נובעים מהורמוני המין המיוצרים בגופם [מקור].
(או רקמה אדיפוזית, Adipose tissue) היא סוג של רקמת חיבור המורכבת מתאים אדיפוציטים – תאי שומן. תפקידה המרכזי של הרקמה הוא אגירת שומן, כלומר אגירת מולקולות עתירות אנרגיה. מזהים שני סוגי רקמה ברורים: רקמת שומן לבנה וחומה [מקור]. תאים אוניאוקולריים אשר מכילים טיפת שומן אחת גדולה, שתופסת את הרוב המוחלט של נפח התא, בעוד גרעין התא נדחק לשולי התא מרכיבים את שכבת השומן הלבן באדם הבוגר. כאשר תאים המולטיאוקולריים שמכילים מספר רב של טיפות שומן מרכיבים את השומן החום.
רקמת שומן חומה עוסקת מבחינה תפקודית בתרמוגנזה, או בייצור חום אדפטיבי, תהליך שכולל ניתוק מוסדר של זרחון חמצוני מיטוכונדריאלי באמצעות נוכחות של חלבון הניתוק הספציפי לרקמות: UCP-1 [מקור] , UCP-1. בעוד שרקמת שומן חומה היא צרכנית נטו של חומצות שומן, שומן לבן הוא האיבר המרכזי לאחסון דלק. התפקיד העיקרי של אחסון הדלק של רקמת השומן הלבנה הוביל לכך שליפוגנזה וליפוליזה נתפסו זמן רב כתהליכים המטבוליים המרכזיים ברקמה.
רקמת השומן, והשומן הלבן בפרט, מופצת באופן נרחב בכל הגוף ונמצאת במספר מאגרים נפרדים, הן תת עורית והן סביב איברים פנימיים, נושא שהוזכר למעלה. בנוסף, אדיפוציטים עשויים להיות מוטמעים בתוך רקמות אחרות כגון סביב סיבי שריר השלד. גיוון מיקום זה נחשב יותר ויותר כמשקף גם המידה של הטרוגניות תפקודית, כאשר שומן קרביים קשור יותר לתסמונת המטבולית ולהפרעות אחרות הקשורות להשמנה.
תהליך פירוק תאי השומן שמתרחש ברקמת השומן גורם לייצורם של טריגליצרידים וחומצות שומן חופשיות [מקור] ובחינת מצבו משמש בבדיקת הדם הפורטלי להערכה של הסטאטוס המטבולי של אדם עם בעיות אנדוקריניות [מקור]. נושא חשוב נוסף שיכול להיחשף מבדיקתם קשור בגמישות העורקים נושא שפרסמתי עליו מאמר עומק – כאן. המתאם בין רמת FFAועמידות לאינסולין, ודרגת הסיכון למחלה קרדיו-וסקולארית , יכולים להיות משענת וכוח עזר בהבנת מצבם של המטופלים הרלוונטיים, נושא שמרחיב את הבנתנו ואת ההשפעות מרחיקות הלכת של ההיפותלמוס על בריאותנו של הלפטין ומעל כולם של התזונה והמזון כתרופה. השמנה בטנית עמוקה מוכרת כיום כמי שתורמת בצורה משמעותית לרמות חומצות השומן החופשיות – FFA – הנמדדות בדם הפורטלי (כלי הדם המוביל דם מהמעיים והטחול אל הכבד טרם חזרתו למחזור הדם.) [מקור]. הקרבה האנטומית שבין רקמת השומן העמוקה לבין הכבד דרך הוריד הפורטלי ((וריד השער של הכבד) גורמת לכבד להיות חשוף לרמות מוגברות של חומצות שומן חופשיות, אף מעבר לרמה הנמדדת בדם הפריפרי [מקור1, מקור2].
ברמה ההיסטולוגית – מבט מזווית של תורת הרקמות, רקמת שומן לבנה נראית פשוטה להפליא במבנה שלה. נראה שיש מעט מלבד אדיפוציטים בוגרים, מלאים בטיפות שומנים בודדות (חד-עיניות) גדולות, וזה בא לידי ביטוי בעובדה שהרקמה עשויה להכיל 85% שומנים במשקל, מה שמאפשר לאגור דלק בצפיפות אנרגיה גבוהה. למרות מראה שטחי, ישנה הטרוגניות תאית ניכרת, כאשר אדיפוציטים בוגרים מהווים לא יותר מ-50% מכלל תכולת התאים של הרקמה. הפשטות הנראית לעין של שומן לבן ברמה היסטולוגית היא חלקית הסיבה לכך שרק לאחרונה הוכרה המורכבות של אדיפוציטים כתאים מפרישים [מקור].
הרקמה השומנית מובנת לנו יותר כיום היא איבר אנדוקריני, מפריש הורמונים. אדיפוציטים לבנים מרכיבים אותה ומשחררים הורמוני חלבון (protein hormones), אותות וגורמים אדיפוקיניים (adipokines), לכולם השפעה על הגוף שלנו עם מגוון רחב של פעולות פיזיולוגיות.
הורמונים שרקמת השומן מייצרת
מספר הורמונים משתחררים מרקמת השומן בהם ארומטאז (aromatase), המעורב בחילוף החומרים של הורמוני המין TNF alpha, IL-6 ולפטין, אלו ההורמונים שמכונים ביחד 'ציטוקינים' והם מעורבים בשליחת מסרים בין התאים plasminogen activator inhibitor-1 – PAI-1 – מעכב משפעל פלסמינוגן – 1, המעורב בקרישת הדם ואנגיוטנסין (פפטיד המשמש כהורמון Angiotensin), המעורב בבקרת לחץ הדם.
אדיפונקטין – adiponectin, הוא האדיפוקין הורמון שמשפר את רגישות הגוף לאינסולין וכך מסייע בהגנה מפני התפתחות סוכרת מסוג 2. הורמון זה משפיע על מטבוליזם של גלוקוז וחומצות שומן[7]. ל אדיפונקטין השפעות מיטיבות כנוגד דלקת[8]. יחד עם זאת, כנזכר למעלה, להבדיל מלפטין, רמות אדיפונקטין בדם מצויות ביחס הפוך למסת רקמת השומן, כלומר ככל שמסת רקמת השומן בגוף גדולה, רמות ההורמון בדם נמוכות יותר. הורמונים נוספים שרקמת השומן מייצרת הם ליפופרוטאין ליפאז ואפוליפופרוטאין E (lipoprotein lipase and apolipoprotein E), המעורבים באחסון ובמטבוליזם של שומן ובשחרור אנרגיה [מקור1, מקור2].
תפקוד לקוי של רקמת השומן נקבע על ידי פגיעה ביכולת ההתרחבות שלה, היפרטרופיה של שומן, חילוף חומרים שומנים ודלקת מקומית.
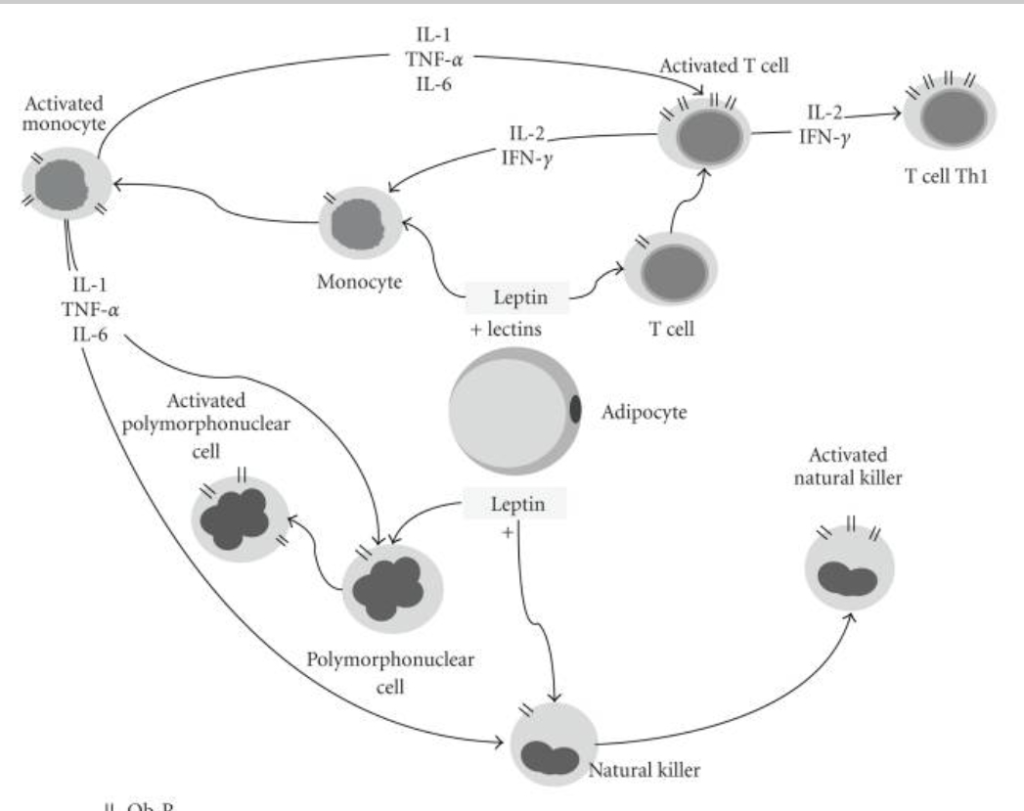
צילום מסך מהמאמר Role of Leptin in the Activation of Immune Cells מאת Patricia Fernández-Riejos,Souad Najib,Jose Santos-Alvarez,Consuelo Martín-Romero,Antonio Pérez-Pérez,Carmen González-Yanes,and Víctor Sánchez-Margalet – כאן.
מחקרים אנושיים עדכניים מצביעים על כך שחמצון רקמת השומן עשוי להיות גורם מפתח כאן. תת-קבוצה של אנשים שמנים – 'השמנת יתר בריאה מבחינה מטבולית' (MHO) – יש תפקוד טוב יותר של רקמת השומן, פחות אחסון שומן מחוץ לרחם, והם רגישים יותר לאינסולין מאשר אנשים שמנים לא בריאים מבחינה מטבולית, תוך שימת דגש על התפקיד המרכזי של תפקוד רקמת השומן בבריאות המטבולית. עם זאת, מחלוקת הקיפה את הרעיון שהשמנת יתר בריאה מבחינה מטבולית עשויה להיחשב בריאה באמת מכיוון שאנשים עם MHO נמצאים בסיכון מוגבר למחלות מטבוליות (קרדיו) ועשויים להיות בעלי איכות חיים נמוכה יותר מאשר נבדקים במשקל תקין עקב מחלות נלוות אחרות. פנוטייפ מטבולי מפורט של אנשים שמנים יהיה בעל ערך רב בהבנת הפתופיזיולוגיה של הפרעות מטבוליות, והוא נחוץ כדי לזהות אנשים או תת-קבוצות בסיכון גבוה, ובכך לסלול את הדרך לאופטימיזציה של אסטרטגיות מניעה וטיפול למלחמה במחלות קרדיומטבוליות [מקור].
ההורמון דמוי הציטוקינים, לפטין, המסונתז בעיקר בשומן לבן, [מקור]
למאמרי
אבחון מוקדם של תפקוד הכליות מאפשר אריכות חיים.
רעלים אורמיים מקדמים דיאליזה – הוכח לאחרונה שרעלנים אורמיים קשורים
למה חולים שנוטלים כדורים להפחתת לחץ דם גבוה, יגיעו בוודאות לדיאליזה – כאן
מאמר חשוב למי שהטיפול בו כשל והוא כבר מופנה לדיאליזה – תובנות חדשות אי-ספיקת כליות תלויה במצבו של ציר FGF23-Klotho –
הולך ומתגלה כגורם הבולט מבין האדיפוקינים השונים הללו כגורם, שאחראי על איזון רקמת השומן ותחושת הרעב. ללא ספק ללפטין תפקיד מרכזי בבקרת התיאבון ואיזון האנרגיה שלנו. יחד עם זאת הלפטין יכול לעבור מוטציות, כאשר מוטציות בגנים המקודדים להורמון או לקולטן שלו נמצאות הן עלולות ואף מובילות להשמנה רצינית בבני אדם [מקור].
לפטין מווסת את התיאבון בעיקר באמצעות אינטראקציה עם מסלולים נוירואנדוקריניים שנמצאים בהיפותלמוס, אשר הוזכרו למעלה: עיכוב פפטידים אורקסיגניים כגון נוירופפטיד (Y (neuropeptide Y) ואורקסין A (orexin A), גם גירוי פפטידים אנורקסיגניים (anorexigenic neuropeptides) כגון פרואופיומלנוקורטין ( proopiomelanocortin – POMC) [מקור1, מקור2, מקור3]. השומן הלבן גם מפריש כמה אדיפוקינים שעדיין נחקרים וקשורים לתיאבון, ביניהם אינטרלוקין-6 (interleukin-6) ואדיפונקטין (adiponectin).
דרך הלפטין והאדיפוקינים האחרים ניכר שרקמת השומן מתקשרת באופן נרחב עם איברים אחרים וממלאת תפקיד נרחב בהומאוסטזיס מטבולי
קיטוב תאי T וחסינות הגוף
עבור תאי Th1 ו-Th2, ללפטין תפקיד חשוב בחסינות הגוף. הוא מאפשר ייצור ציטוקינים מסייע T תאים אלו מפרישים ציטוקינים הגורמים לגיוס אלמנטים שונים למאבק בפתוגן שנכנס לגוף [מקור]. נמצא כי
ללפטין גם תפקיד החשוב ביותר בחסינות הגוף. מחקר מצא שלפטין הוא Th17 הכרחי להתמיינות לימפוציטים;
ללפטין פונקציות אנדוקריניות וחיסוניות וככזה הוא מגביר את הפרשת הציטוקינים הפרו-דלקתיים על ידי תאי מערכת החיסון [מקור].
הקשר בין מצב תזונתי לכשירות חיסונית עובר דרך הלפטין. Adipose tissue רקמת שומן היא איבר אנדוקריני פעיל שמפריש כנרשם למעלה הורמונים שונים (אדיפוקינים) [מקור]. המעבר של רקמת השומן לייצור ציטוקינים פרו-דלקתיים בהשמנת יתר תורם ככל הנראה לדלקת מערכתית ברמה נמוכה שעלולה להיות נוכחת בפתולוגיות כרוניות הקשורות לתסמונת מטבולית כמו טרשת עורקים ואבדן גמישות העורקים. לפטין הוא אחד ההורמונים החשובים ביותר המופרשים על ידי אדיפוציטים, שמרכיבים את ריקמת השומן. עם מגוון תפקידים פיזיולוגיים הקשורים בשליטה על חילוף החומרים והומאוסטזיס אנרגטי. אחד מהפונקציות הללו הוא הקשר בין מצב תזונתי לכשירות חיסונית. ההורמון לפטין שמקורו באדיפוציטים הוכח כמווסת את התגובה החיסונית, התגובה המולדת והסתגלנית, הן במצב נורמלי והן במצב פתולוגי. תפקידו של הלפטין בוויסות התגובה החיסונית הוערך במבחנה וכן במחקרים קליניים. הוכח שמצבים של ייצור לפטין מופחת קשורים לרגישות מוגברת לזיהום. לעומת זאת, הפרעות בתיווך חיסוני כגון מחלות אוטואימוניות קשורות להפרשה מוגברת של לפטין ולייצור ציטוקינים פתוגניים פרו-דלקתיים. לפיכך, לפטין הוא מתווך של התגובה הדלקתית.
בנוסף, יש צורך בהתמיינות של לפטין ותימוציטים ( תא חיסון של התימוס [מקור]) מdouble-positive cells (CD4+CD8+) ל-CD4+ של Treg (טרג Treg– תאי אסדרה, מסייעים להסדיר פעולות בגוף כלומר הם סוגים של תאי רגולטורים ) הקשורים לתאים חיוביים בודדים כדי לדכא את התגובה החיסונית החריגה במחלות אוטואימוניות [מקור1, מקור2, מקור3, מקור4]. המפתח נמצא במהלך הזה בלפטין. הוא שמעכב CD4+CD25+ [מקור]. כאשר Treg מתרבה, הקולטן ללפטין (LEPR) גדל. כמות הלפטין הקיימת אז על פני תאי האסדרה Tregs פירושה שטיפול חוסם לפטין במבחנה יכול לגרום לשגשוג של Treg. בנוסף, מחקרים מצאו שבקרב עכברים חסרי לפטין (עכברי ob/ob) ועכברים חסרי LEPR (עכברי DB/DB), מספר ה-Tregs עולה באופן משמעותי [מקור1, מקור2, מקור3]. במונחים של עיכוב אקטיבי של התפשטות Treg, המחקר מצא כי בעכברי נוקאאוט LEPR, פעילות mTOR נמוכה מזו של עכברים רגילים, מלווה בשגשוג Treg [מקור]. בנוסף, לפטין יכול לעכב תהליכי נורמה של CD4+CD25 בגוף האדם. לגבי תהליך האוטופגיה בתאי T, ציר הלפטין-mTOR הוא מופיע כקשר פוטנציאלי בין חסינות ומצב אנרגיה. כמו כן, תאים מבטאים LEPR מוארך על פני התא, מה שמצביע על כך שלפטין משפיע באופן חיובי על לימפוציטים מסוג B [מקור].
דגירה של תאי B במעבדה, תאים שנלקחו דגירה של תאי B מאנשים צעירים רזים עם לפטין נבחנה בניסוי שנערך במעמבדה [מקור], נמצא כמי היא מגבירה את התדירות של תאי B פרו-דלקתיים אותם תאים שעומדים בעורף המערכה מול פולשים, מייצרים מיליוני נוגדנים, מאפשרים לחיסונים שאנחנו מקבלים לפעול כשהגוף מותקף באמת. כך הם מעוררים דלקת פנימית של תאי B, המאופיינת בביטוי mRNA של ציטוקינים פרו-דלקתיים (TNF-α ו-IL-6), כימוקינים. מספר הלימפוציטים מסוג B מצטמצם. הלימפוציטים מסוג B מכונים גם תאי-B. ם אחראים ליצירת נוגדנים (מכונה גם התגובה ההומוראלית). הם נוצרים במח העצם ועם הבשלתם מגיחים למערכת הלימפה, דרכה הם מגיעים לחלקי הגוף השונים. החוקרים הראו כי לאחר טיפול בלפטין, וספירת תאי B עולה, ההגנה או יכולת ההגנה של הגוף משתפרת. לפטין מתבטא אז בהפעלת BCL-2, ו-cyclin D1 מושרה למחזור התא. הוא מקדם שגשוג לימפוציטים B ומעכב אפופטוזיס של מחזור התא באמצעות אותות JAK-STAT ו-p38 MAPK-ERK1/2 [מקור1, מקור2]. נושא זה גם משרה ציטוקינים פרו-דלקתיים (כגון גורם נמק של גידול (TNF) ואינטרלוקין 6 (IL-6)) וציטוקינים מווסתים אנטי דלקתיים וחסוניים IL-10 [מקור]. יתר על כן, לפטין יכול להגדיל את מספר תאי B על ידי קידום שגשוג והפחתת קצב האפופטוזיס. כך הלפטין שב ומוכח כהורמון חשוב שמשמש גם כמפעיל תאי B ומי שמעודד הפרשה של ציטוקינים שבאים לווסת מצבים פרו-דלקתיים ואנטי-דלקתיים. יתרה מכך, היווצרות תאי B [מקור].
לפטין משחק תפקיד בהתפתחות של מספר הפרעות אוטואימוניות [מקור].
המבנה של הלפטין וגם זה של הקולטן שלו מצביעים על כך שלפטין עשוי להיות מסווג כציטוקין [מקור]
רצף חומצות האמינו הראשוני של לפטין מצביע על כך שהוא משתייך למשפחת הציטוקינים הסליליים ארוכי השרשרת [מקור], כך למשל נמצאו גורם נמק גידולי-α, אינטרלוקין (IL)-2, IL-12 ו-GH [מקור]. הוא אחד ממשפחה של מולקולות חלבון קטנות פעילות ביולוגית הידועות כציטוקינים. IL-6 הוא למעשה ציטוקין נוגד דלקת אך באותה עת גם מעודד דלקת, המשתחרר ממגוון של רקמות, כולל לויקוציטים משופעלים, פיברובלסטים, מונוציטים, מקרופאגים, תאי T, אדיפוציטים, תאי אנדותל, וכן על ידי תאי סרטן אחדים [מקור]. למעשה, קולטן ללפטין (Ob-R) מראה הומולוגיה של רצף למרכיבים ביולוגיים ממשפחת קולטני ציטוקינים מסוג I (gp130) [מקור] הכוללת את הקולטן ל-IL-6, גורם מעכב לויקוציטים (LIF) ואת גורם מגרה מושבה גרנולוציטים (G-CSF). יתר על כן, הוכח כי הקולטן ללפטין (Ob-R) הוא בעל יכולות איתות של קולטני ציטוקינים מסוג IL-6 [מקור], שמפעילים מסלולי איתות של JAK-STAT – מסלול האיתות JAK-STAT הוא שרשרת של אינטראקציות בין חלבונים בתא. מסלול זה מעורב בתהליכים כמו חסינות, חלוקת תאים, מוות תאים ויצירת גידול. המסלול מתקשר למידע שמגיע מאותות כימיים מחוץ לתא לגרעין התא, וכתוצאה מכך מתרחשת הפעלה של גנים בתהליך של שעתוק., PI3K הם משפחה של אנזימים המעורבים בתפקודים תאיים כגון צמיחת תאים, שגשוג, התמיינות, תנועתיות, הישרדות וסחר תוך תאי, אשר בתורם מעורבים במחלת הסרטן. PI3Ks הם משפחה של אנזימים מתמירי אותות תוך תאיים. הם מסוגלים לזרחן את קבוצת ההידרוקסיל במיקום ה-3 של טבעת האינוזיטול של פוספטידילינוזיטול (PtdIns).[מקור] המסלול, עם האונקוגן PIK3CA וגן מדכא הגידול PTEN, שמעורב ברגישות של גידולים סרטניים לאינסולין ו-IGF1, ובהגבלת קלוריותו–MAPK – חלבון קינאז המופעל על ידי מיטוגן (MAPK או MAP kinase) הוא סוג של חלבון קינאז. חלבון ספציפי לחומצות האמינו סרין ותריונין (כלומר, חלבון קינאז ספציפי לסרין/תרונין). MAPKs מעורבים בהכוונת תגובות תאיות למערך מגוון של גירויים, כגון מיטוגנים, מתח אוסמוטי, הלם חום וציטוקינים מעודדי דלקת. הם מווסתים את תפקודי התא, לרבות שגשוג, ביטוי גנים, התמיינות, מיטוזה, הישרדות תאים ואפופטוזיס[מקור1, מקור2]. בהקשר לנושא האחרון, הוצע תפקיד ללפטין בוויסות החסינות המולדת [מקור1, מקור2]. ובהתאם לתפקיד זה של הלפטין המשפיע על מנגנוני התגובה החיסונית והגנת המארח, רמות הלפטין במחזור מוגברות בעקבות גירויים זיהומיים ודלקתיים כגון LPS, טרפנטין (turpentine)וציטוקינים (cytokines) [מקור1, מקור2]. מצד שני, בניגוד לחברים אחרים במשפחת IL-6, לא ברור שלפטין עשוי לגרום לביטוי של חלבונים בשלב אקוטי [מקור1, מקור2].
לפטין ממלא תפקיד בחסינות מולדת ונרכשת. רמות הלפטין עולות בצורה חריפה במהלך זיהום ודלקת. מחסור בפטין בעל משמעות גדולה לבריאותנו כי המחסור בלפטין מגביר את הרגישות לגירויים זיהומיים ודלקתיים. מחסור בלפטין קשור לחוסר ויסות של ייצור ציטוקינים. מחסור בפטין גורם גם לפגם בהמטופואזה. לפטין מווסת את התגובות של תאי T, ומקטב תאי Th לכיוון פנוטיפ Th1. רמות לפטין נמוכות המתרחשות במהלך רעב מתווכות את התפקוד הנוירואנדוקריני והחיסוני של הרעב [מקור].
תת תזונה פוגעת בתפקוד החיסוני, מפחיתה את העמידות לזיהומים.
[מקור].
רמות הלפטין יורדות במהירות עם תחילת הרעב, וזאת באופן לא פרופורציונלי לשינויים במסת רקמת השומן.
[מקור]
ירידה בלפטין המושרה על ידי רעב מגבירה את הרגישות לתמותה המושרה על ידי ליפופוליסכריד (LPS) ו-Tumor necrosis factor (TNF) [מקור]. נושא זה עולה ומשתקף מניסויים בחיות מעבדה, צום של 48 שעות מגביר את הרגישות ל-LPS. הפחתת הנפילה הזו של לפטין, אשר מקורה בצום על ידי מתן לפטין לימדה את החוקרים כי הרעב מעלה באופן ניכר את הרגישות ל-LPS, אך תוסף של לפטין מאזן אותו. למרות שצום מפחית את רמות הלפטין הבסיסיות, טיפול ב-LPS הראה שינוי באותה מידה שניכר בקרב בעלי חיים שהוזנו כראוי.
לפטין החזיר את תגובת הקורטיקוסטרון ל-LPS. רמות הגלוקוז בסרום ירדו בעכברים בצום ו-LPS גרמה לירידה נוספת. טיפול לפטין לא השפיע לא על הגלוקוז הבסיסי ולא על זה לאחר LPS. LPS גרמה לעלייה גדולה פי חמישה ב-TNF בסרום בעכברים בצום, שהוקהה על ידי תחליף לפטין. לעומת זאת, LPS גרמה לרמות נמוכות יותר של אינטרפרון-γ וללא הבדלים באינטרלויקין-1β בצום בהשוואה לבעלי חיים שניזונו; ללפטין לא הייתה השפעה על הציטוקינים האלה. יתר על כן, צום הגביר את הרגישות להשפעה הקטלנית של ה-TNF עצמו, שגם הוא התהפך על ידי טיפול בלפטין. לפיכך, נראה לחוקרים בשלב זה שלפטין מגן הן על ידי עיכוב השראת TNF על ידי LPS והן על ידי הפחתת רעילות TNF.
בשנת 2013 אושר ביפן (תחילה) שימוש בלפטין כתרופה. כיום אנלוגי לפטין היו להורמון מאושר לשימוש גם בארצות הברית לטיפול במחסור מולד של לפטין [מקור]. הוא מיועד לטיפול בהשמנת יתר ו/או מחסור בלפטין. במקרים אחדים נמצא שלפטין עשוי לשמש לסוכרת והיפר-טריגליצרידמיה [מקור].
נשארו לך שאלות
אשמח להשיב על כל שאלה
לטופס פנייה ישירה אל ירון מרגולין – נא להקליק – כאן
בבקשה לא להתקשר משום שזה פשוט לא מאפשר לי לעבוד – אנא השתמשו באמצעים שלפניכם –
למען הסר ספק, חובת התייעצות עם רופא (המכיר לפרטים את מצבו הבריאותי הכללי של כל מטופל או שלך) לפני שימוש בכל תכשיר, מאכל, תמצית או ביצוע כל תרגיל. ירון מרגולין הוא רקדן ומבית המחול שלו בירושלים פרצה התורה כאשר נחשפה שיטת המחול שלו כבעלת יכולת מדהימה, באמצע שנות ה – 80 לרפא סרטן. המידע באתר של ירון מרגולין או באתר "לחיצות ההחלמה" (בפיסבוק או MARGOLINMETHOD.COM ), במאמר הנ"ל ובמאמרים של ירון מרגולין הם חומר למחשבה – פילוסופיה לא המלצה ולא הנחייה לציבור להשתמש או לחדול מלהשתמש בתרופות – אין במידע באתר זה או בכל אחד מהמאמרים תחליף להיוועצות עם מומחה מוכר המכיר לפרטים את מצבו הבריאותי הכללי שלך ושל משפחתך. מומלץ תמיד להתייעץ עם רופא מוסמך או רוקח בכל הנוגע בכאב, הרגשה רעה או למטרות ואופן השימוש, במזונות, משחות, תמציות ואפילו בתרגילים, או בתכשירים אחרים שנזכרים כאן.
מאמרים אחרונים
- חילוף חומרים אנרגטי, איזון רקמת השומן ובקרת תיאבון – על כוחו של הורמון לפטין
- מלטונין הוכח שהורמון השינה נוגד חמצון רב עוצמה ויעיל כתרופה בקרב חולי כליה
- מיטוכונדריה – במיטוכונדריון מתחילה מחלת הכליות
- התקף לב / אירוע לבבי בעקבות מחלת כליות – מסלול איתות שמגן על הלב בשם "VEGFA" משתבש בגלל מחלת כליות כרונית.
- סמנים ביולוגיים (Novel Biomarkers) ובדיקת כליות מוקדמת ככל האפשר – מצילה חיים
- אבחון מוקדם של תפקוד הכליות מאפשר אריכות חיים.
- חומוס מזין, מרגיע ונוגד חרדות – מתכונים
- חרדה וצ'יפס
- רוצה להחלים מאי ספיקת כליות – יש להגיע לטיפול מחלים כליות מהר ככל האפשר
- הצלבת איברים – הדרך להחלמה ממחלת כליות קשה מאוד
- רוצה להחלים ללא תרופות ממחלת מחלת כליות נפרופתיה אימונוגלובולין איי?
- ממצאים חדשניים למקור הגאוט
- צרבת כרונית – רוצה להחלים ללא תרופות?
- יתר שומנים בדם היפרליפידמיה – חשש לצורך בצנתור
- מהי תסמונת מטבולית (MetS)?
- חדשות הרפואה – חוקרים יצרו דרך לזהות את סרטן הלבלב (PC) וגם את התפתחותו של סרטן הערמונית באמצעות בדיקת שתן, בדיקה שיכולה לסייע בגילוי מוקדם.
- מחסור ביוד, חוסר סלניום או עודף פלואור במים גם דמימה בשרירים שנצמדים לעצם הלשון עלולים להוביל לתת פעילות של בלוטת התריס (תירואיד)
- מסלול איתות חדש במוח שמווסת אכילה מופרזת
- דיכאון וחרדה בקרב חולי כליות
- עורקים גמישים – הסוד והדרך לזכייה בבריאות מחדש
- יש פתרון כולל לבעיות הקשורות לדימוי עצמי, חוסר בטחון וערך עצמי נמוך – דופמין
- שיחות ההחלמה ושיחות בין ידידים – על ההבדלים ביניהן
- משחה צהובה – לכאבי שרירים – משחת הפלא להפחתת כאבים
- לסדרת מאמרי – מבוא לתורת הגוף-נפש המודרנית – חלק א
- הפסיכולוגיה הטיפולית וההוליסטית – תולדות הפסיכותרפיה
- הגיל השלישי, תאוותיה של הזיקנה – ואיך להתבגר יפה, טוב ובריא
- בני-על – האם יש גבול ביולוגי למספר השנים שאדם יכול לחיות?
- כל מה שאתה צריך לדעת על מיקרו-תזונה – ויטמינים ומינרלים
- הפרעה אנדוקרינית
- חרדה
- מגילת רות האלמנה שיצאה ממרחב הנוחות
- איך מורידים לחץ וחרדות באופן טבעי? התמודדות עם סטרס ולחץ נפשי
- טיפול נפשי ללא תרופות – חרדות, פחדים וייאוש – תסמינים שיש להם פתרון טבעי, מדויק ומהיר
- מסלול ההתפתחות הנורמטיבי בחיי אדם ודמימותיו בטבלה – סדרת מאמרים.
- למה אני לא מצליח להתמיד – והסוכר
- על ההזנחה –
- גמישות היא מצב נפשי – אתגר בזרימה ושינוי – אני מבקש להתגמש
- חזרה לבסיס – עקרונות צירופי המזון
- ניתוק רגשי – על הקורוציונה
- די לכאב
- ראיית המעמקים – כניסה לטרקלין או על החיים האמתיים.
- התודעה השלילית
- ביקורת מבזה
- איך לצאת ממצבי תקיעות בחיים – שיטת שלוש השאלות בגובה העיניים
- נמאס לי מהחיים מה עושים
- על היכולת להשתקם, לקום מאבק הדרך ומכאב הפרידה
- ירקות ירוקי עלים לרוב טובים לבריאותנו, לפעמים הם לא – רוצה לדעת מתי כדאי לצרוך עלים ירוקים?
- תרופות ללחץ דם גבוהה נמצאו כקשורות לסיכון מוגבר לסכיזופרניה
- מדד חדש לבריאותך – ביטול האסרוסקלרוזים
- לראשונה, מדענים הצליחו לתרגם לטקסט את הפעילות המוחית של אדם עם שיתוק שאינו מסוגל לדבר.
- רוצה להחלים בצורה פשוטה ביותר, ללא תרופות ממחסור בטסטוסטרון או מירידה במדד ה SHBG ?
- אוראה – למה האוראה מוגברת ומופחת בדם Urea
- טיפולים מבוססי רירית לזיהומים נגיפיים וחיידקיים
- מחסור בברזל
- קרום התא – הממברנה והדלקת הכרונית
- מחלת שינוי מינימלי Minimal Changes Disease מינימל צ'יינג'
- מה היא בדיקת D-dimer
- חלב לקוליטיס כיבית: כל מה שחשוב לדעת
- המפריעון Vaxinia – CF33 בפעם הראשונה הוזרק בניסוי קליני וירוס קוטל תאי סרטן.
- סטרס יכול לעתים גם לרפא – מחקר חדש על תאי המוח
- רככת היפופוספטמית (זרחן נמוך מהנורמה) – מחלת כליות כרונית – או הפרעת עצם מינרלית
- אי ספיקת כליות – הגורמים השכיחים ביותר ל-CKD הם סוכרת שנשלטת על ידי תרופות = שליטה גרועה בסוכרת ויתר לחץ דם שמטופל לכאורה על-ידי תרופות
- מחלת כליות פוליציסטית אוטוזומלית דומיננטית (ADPKD)
- גמילה מאלכוהול – תהליך קשה, תסמינים איומים
- הגל החדש של בדיקות דם בהחלט רוצה לייעל את הביצועים הספורטיביים שלך, לשפר את הרווחה הכללית ולהרחיב או להאריך את תוחלת החיים גם לסייע להחלמתך ללא תרופות ממחלות כרוניות
- מדללי דם טבעיים – חומרים אנטי-תרומבוטיים: נאטוקינאז, ויטמין E, פלפל קאיין, כורכום, קינמון, וספורט מאפשרים טיפול בנוזלי הדם ללא תרופות.
- סלניום Se התגלה כאנטי- אייג'ינג ומגן מפני מחלות כרוניות
- מהו אימון שלפוחית השתן?
- פסוריאזיס, האם הימנעות מגלוטן מסייעת לחולי הפסוריאזיס
- חלב לקוליטיס כיבית: כל מה שחשוב לדעת
- המפריעון Vaxinia – CF33 בפעם הראשונה הוזרק בניסוי קליני וירוס קוטל תאי סרטן.
- סטרס יכול לעתים גם לרפא – מחקר חדש על תאי המוח
- רככת היפופוספטמית (זרחן נמוך מהנורמה) – מחלת כליות כרונית – או הפרעת עצם מינרלית
- אי ספיקת כליות – הגורמים השכיחים ביותר ל-CKD הם סוכרת שנשלטת על ידי תרופות = שליטה גרועה בסוכרת ויתר לחץ דם שמטופל לכאורה על-ידי תרופות
- מחלת כליות פוליציסטית אוטוזומלית דומיננטית (ADPKD)
- גמילה מאלכוהול – תהליך קשה, תסמינים איומים
- הגל החדש של בדיקות דם בהחלט רוצה לייעל את הביצועים הספורטיביים שלך, לשפר את הרווחה הכללית ולהרחיב או להאריך את תוחלת החיים גם לסייע להחלמתך ללא תרופות ממחלות כרוניות
- מדללי דם טבעיים – חומרים אנטי-תרומבוטיים: נאטוקינאז, ויטמין E, פלפל קאיין, כורכום, קינמון, וספורט מאפשרים טיפול בנוזלי הדם ללא תרופות.
- על הנקמה – פנטזיות נקמה לאחר חווית אירועים טראומטיים
- מסלול ההתפתחות הנורמטיבי בחיי אדם ודמימותיו בטבלה. עמוד 18
- מסלול ההתפתחות הנורמטיבי בחיי אדם ודמימותיו בטבלה. עמוד 17
- המפריעון Vaxinia – CF33 בפעם הראשונה הוזרק בניסוי קליני וירוס קוטל תאי סרטן.
- סטרס יכול לעתים גם לרפא – מחקר חדש על תאי המוח
- אי ספיקת כליות – הגורמים השכיחים ביותר ל-CKD הם סוכרת שנשלטת על ידי תרופות = שליטה גרועה בסוכרת ויתר לחץ דם שמטופל לכאורה על-ידי תרופות
- גאוט הוא לא רק יתר פורין – החיים עם גאוט תלוי גיל ומין – האם אפשר לנצח גאוט בלי לבלוע הורמוני מין?
- גלוטתיון כל האמת
- תרופות הרגעה שמשאירות אותך רעב וחרד – ציפּרָלֵקס, פּרוֹזַק, פלואוקסטין
- גלוטמין (Gln) -המגן הגדול על בריאות האדם – כל מה שחשוב לדעת
- פיקנוגנול – כל האמת על רפואת עץ האורן והכנת התה ממחטיו
- תחמוצת החנקן (NO) כיווץ תאי האנדותל, מחלות כרוניות קשות – ודרכי ריפוי חדשות
- מחשבון מדידה והערכת קצב הסינון הגלומרולרי (GFR) אשר מבוסס על קריאטינין, נתוני גוף, גיל, גזע ומין.
- אומגה 3 צמחית (שמן חרדל, שמן מרווה מרושתת) עולה על צורות אחרות של אומגה 3 ויש והן לבדן תורמות לבריאות בעוד האחרות עלולות להזיק יותר משלהועיל לך
- התכנית לשיקום הכליות פרק ז' – עקרונות הטיפול
- התכנית לשיקום הכליות פרק ו' – התבוננו אל מדד האוראה
- התכנית לשיקום הכליות פרק ה' תנגודת לאינסולין
- התכנית לשיקום הכליות פרק ד'
- התכנית לשיקום הכליות פרק ג
- התכנית לשיקום הכליות פרק ב
- התכנית לשיקום הכליות – פרק א'
- אכל נקי
- אי ספיקת כליות – טיפול ללא תרופות
- על ההשפעה האיומה של חלבון מן החי על הכליות
- אילוף הכליות הסוררות
- גודש נוזלים בריאות – בקרב חולי כליה
- עשרת המזונות הבריאים ביותר לחולי כלייה – קמח קליפת רימונים (PPF) .9
- הגיל השלישי, תאוותיה של הזיקנה – ואיך להתבגר יפה, טוב ובריא
- רוצה להחלים בצורה פשוטה ביותר, ללא תרופות ממחסור בטסטוסטרון או מירידה במדד ה SHBG ?
- רעלים אורמיים מקדמים דיאליזה – הוכח לאחרונה שרעלנים אורמיים קשורים למיקרוביוטה של המעי הגס – איך להחלים ללא תרופות ולהימנע מדיאליזה.
- רככת היפופוספטמית (זרחן נמוך מהנורמה) – מחלת כליות כרונית – או הפרעת עצם מינרלית.
- גודש נוזלים בריאות – בקרב חולי כליה
- דלקת כליות אינטרסטיציאלית – השתמשו במי שעורה
- יתר לחץ דם – שינוי פרדיגמה וגישות חדשות – לחץ דם גבוה וטיפול טבעי ללא תרופות לאחר שטיפול תרופתי נערץ כשל
- הומוציסטאין, ויטמינים ומניעת מחלות כלי דם
- פרפור פרוזדורים (A-fib) יכול להפסיק מעצמו.
- טיפול בכאב עם אופיואידים גורר אותך לצרות צרורות למשל עצירות איומה. מה לעשות?
- גאוט הוא לא רק יתר פורין – החיים עם גאוט תלוי גיל ומין – האם אפשר לנצח גאוט בלי לבלוע הורמוני מין?
- חומצה אלפא לינולנית משפרת את תוחלת החיים – צריכה גבוהה של חומצות שומן מצמחים נחשפה כגורם שמאריך את החיים.
- תובנות חדשות אי-ספיקת כליות תלויה במצבו של ציר FGF23-Klotho
- Tsamba שתי כוסות גרגרי שעורה דגנים מלאים, רצוי אורגניים – מתכון צ'מפה למבקשים להחלים מאי ספיקת כליות
- פאראצטמול (PARACETAMOL) גם פרצטמול או אצטאמינופן (Acetaminophen) – הידוע גם בשם אקמול, רוקסט ודקסמול עלול לפגוע בכליות ובכבד ואסור לשימוש לחולי כליה
- מקצבים בעולם החי – שעון ביולוגי בתאי הגוף
- מעגל המוזר – התפתחות ה"אני" בשנה התשיעית לחייו

כתיבת תגובה